摘要
目的
评估电阻抗断层扫描(EIT)与传统方法比较在优化急性呼吸窘迫综合征(ARDS)患者呼气末正压(PEEP)中改善呼吸系统力学和预防呼吸机相关性肺损伤(VILI)的有效性。
方法
通过系统综述与Meta分析整合2012年1月至2023年5月ScoPus、PubMed、MEDLINE(Ovid)、Cochrane及LILACS数据库的文献。纳入13项研究(3项随机对照试验、10项非随机研究),共623例符合柏林定义的ARDS患者。采用随机效应模型评估EIT引导的PEEP策略与传统方法(如ARDSNet PEEP/FiO2表、压力-容积曲线分析等)对主要结局(肺顺应性、机械功、驱动压)及次要结局(PaO2/FiO2比值、死亡率、ICU停留时间、无呼吸机天数)的影响。
结果
相较于传统方法,EIT引导的PEEP显著优化呼吸力学参数:肺顺应性提升(n=941,MD=4.33,95% CI [2.94, 5.71])、机械功降低(n=148,MD=−1.99,95% CI [−3.51, −0.47])、驱动压下降(n=903,MD=−1.20,95% CI [−2.33, −0.07])。敏感性分析显示,随机与非随机研究合并后,EIT对肺顺应性的改善趋势仍存在(MD=2.43,95% CI [−0.39, 5.26])。此外,三项研究提示EIT组死亡率显著降低(n=259,RR=0.64,95% CI [0.45, 0.91]),且与驱动压及顺应性改善呈相关性。
结论
电阻抗断层成像(EIT)能够实现实时、个体化的呼气末正压(PEEP)调整,从而改善呼吸系统力学。将EIT作为指导工具整合到机械通气策略中,在预防呼吸机相关肺损伤方面具有潜在优势。未来需要通过更大规模的临床研究来验证和优化EIT在急性呼吸窘迫综合征(ARDS)管理中的临床应用价值。
关键词
机械通气,呼吸机相关性肺损伤, ARDSNet
背景
急性呼吸窘迫综合征(ARDS)作为临床危重症,其死亡率高达35%-45%,核心病理特征为急性呼吸衰竭。机械通气虽是ARDS患者生命支持的关键手段,但可能因通气压力不当引发呼吸机相关肺损伤(VILI),这一矛盾凸显了个体化通气策略对改善预后的重要性。
在ARDS管理中,呼气末正压(PEEP)的合理应用对维持肺泡复张和改善氧合具有关键作用。目前临床实践中广泛采用的ARDSNet PEEP/FiO2标准化方案虽已成为治疗基准,但针对最佳PEEP水平的争议持续存在。尽管基于肺顺应性、跨肺压及压力-容积曲线拐点等参数的个体化调节方法已被探索,但ARDS患者显著的肺部异质性导致这些传统方法难以实现真正意义上的精准优化。
传统的呼气末正压(PEEP)水平的设定通常采用常规策略,例如ARDSNet PEEP/FiO2表,这已成为ARDS管理的标准方法。尽管已探索了多种个性化PEEP的方法,包括肺顺应性、跨肺压和压力-容积曲线上的拐点,但这些方法并未充分考虑ARDS患者肺部疾病的异质性,因此可能并不适用于所有ARDS患者。近年来,电阻抗断层成像(EIT)作为一种非侵入性成像技术,能够提供实时的区域性肺部信息,已成为指导PEEP设置的潜在工具,用于个体化干预,可能改善ARDS患者的呼吸力学(这是呼吸机相关肺损伤的关键决定因素)。
尽管EIT(电阻抗断层成像)引导的PEEP(呼气末正压)滴定具有潜在优势,但其与传统PEEP滴定方法的有效性对比仍不明确。为了更全面地理解这些方法并指导临床医生为ARDS(急性呼吸窘迫综合征)患者提供最佳监护,我们进行了一项荟萃分析,比较了EIT引导的PEEP滴定与传统方法在改善呼吸系统力学和降低呼吸机相关肺损伤(VILI)风险方面的效果。
材料与方法
数据来源
本研究系统检索了ScoPus、PubMed、Ovid-MEDLINE、Cochrane对照试验中心注册库及LILACS数据库,时间跨度为2012年1月至2023年5月1日。检索策略结合以下关键词组合:(EIT或“电阻抗断层扫描”)与(ARDS或“急性呼吸窘迫综合征”或“急性呼吸衰竭”或“急性肺损伤”)及(“机械通气”或PEEP或“正压呼气末正压”或“肺泡复张”或“潮气量”),限定于标题、摘要及关键词字段。纳入2012年后发表的人类研究,无语言限制。此外,通过手工筛查符合条件文献的参考文献列表,补充潜在相关研究。
研究选择
纳入标准为:基于柏林定义的成年ARDS患者,接受有创机械通气,并比较EIT引导的PEEP选择与传统PEEP调整方法的随机对照试验(RCT)或非随机研究(NRS),且至少报告一项主要或次要结局指标(如呼吸力学参数、PaO2/FiO2、死亡率等)。传统方法定义为ARDSNet FiO2/PEEP表、压力-容积(PV)曲线分析、跨肺压调节等。排除病例报告、病例系列、会议摘要、综述、缺乏对照组的研究,以及仅将EIT用于监测的非干预性研究。
主要结局评估了呼吸系统力学指标,包括肺顺应性、驱动压(DP)、平台压、PEEP水平以及机械功率(MP)。次要结局包括PaO₂/FiO₂比值、28天全因死亡率、院内死亡率、重症监护病房(ICU)住院时间、无呼吸机天数,以及研究作者报告的基于EIT的肺力学指标。这些EIT指标包括“静默区域”百分比(用于量化低通气肺单位)和通气分布系数(%COV),后者表示沿重力轴的通气分布情况。
数据提取与质量评估
由两名独立评审员(NS和CL)通过标题/摘要初筛及全文复筛确定最终纳入文献,争议由领域专家(LB和HZ)仲裁。采用标准化表格提取数据,包括患者人口学特征、研究设计、干预措施及结局指标,并由双人交叉核对。未补充索取未公开数据。RCT的偏倚风险采用Cochrane ROB-2工具评估,非随机研究采用ROBINS-I工具,结果分为低、中、高风险,争议通过共识解决。
使用标准化表格从纳入的研究中提取数据,由一位作者(NS)进行提取,另一位作者(CL)对数据进行交叉检查。信息包括患者特征(人口统计学和临床)、研究人群、干预和控制PEEP滴定策略以及结果(呼吸系统力学测量、 PaO2 /FiO2比值、死亡率、住院时间和无呼吸机天数)。我们除了已发表文章中公开的数据外,没有寻求补充数据。两位作者(NS、CL)独立评估了每项研究的偏倚风险(ROB)。Cochrane ROB-2工具用于随机对照试验,而非随机干预研究中的偏倚风险(ROBINS-I)工具用于非随机对照试验。ROB被分为低、有点令人担忧或高,分歧通过共识解决。
数据综合
使用Review Manager Web软件进行随机效应模型Meta分析,以风险比(RR)和均数差(MD)分别综合分类与连续变量结局,均报告95%置信区间(CI)。中位数数据经转换估算均值和标准差。统计显著性定义为双侧P≤0.05。异质性通过卡方检验(P≤0.1为显著)及I²统计量评估(I²≥50%为显著异质性)。当纳入研究≥10项时,使用Stata进行Egger检验及漏斗图分析评估发表偏倚。
敏感性与亚组分析
敏感性分析聚焦RCT质量、高偏倚风险研究、肺泡复张操作对PEEP的影响、显著阳性结果研究、肥胖患者亚组,以及不同PEEP调整策略(如EIT vs. ARDSNet表、ODCL方法 vs. 传统策略)。亚组分析针对异质性来源(I²≥50%),按患者特征(年龄、BMI、ARDS病因、COVID-19状态、严重程度、机械通气时长)及干预参数(潮气量、复张操作、PEEP调整方向)分层。卡方检验(P≤0.1)评估亚组差异显著性,结合样本量、交互作用及混杂因素决定结果呈现。所有分析仅纳入数据完整且样本量≥10项研究的结局。根据我们的异质性标准,我们将亚组分析指向以“实质性异质性”(I2值在50%至90%之间)和“相当不均匀性”(I2值在75%至100%之间)为特征的实例。根据参与者特征(年龄、体重指数、ARDS病因、2019冠状病毒病(新冠肺炎)、ARDS严重程度、数据收集前机械通气持续时间、纳入前机械通气的持续时间)和研究干预措施(潮气量、复张策略、递增/递减PEEP 、常规干预、)进行亚组分析。使用异质性卡方检验评估亚组效应(P值≤0.1表示显著性)。考虑因素包括每个亚组的试验和参与者数量、相互作用的合理性、相互作用重要性和潜在的混杂因素,这些因素指导提出或省略亚组分析的决定。
结果
研究筛选
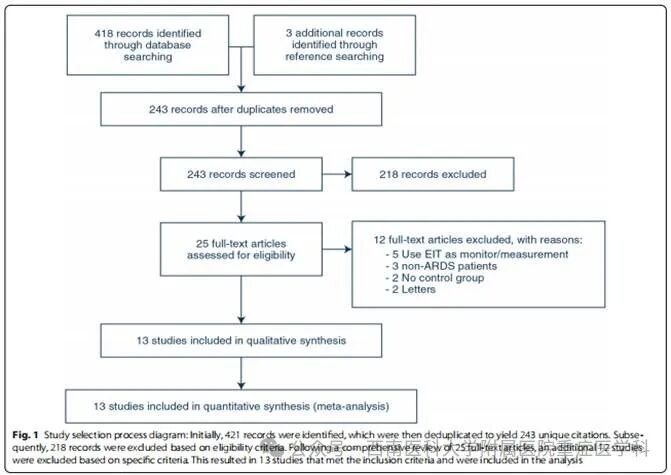
通过数据库检索共获得421条文献记录,剔除重复后保留243项独立研究。经标题/摘要初筛排除218项不符合纳入标准的研究后,对25篇全文进行深度评估,最终排除12项研究(排除原因包括:仅用EIT监测肺功能、纳入非ARDS人群、缺乏对照组或关键数据缺失),最终纳入13项研究(共623例患者)进行Meta分析(图1)。
纳入研究特征
13项研究中,3项为随机对照试验(RCT),10项为非随机研究(NRS)。4项研究聚焦COVID-19相关ARDS患者。患者平均年龄范围为41-70岁,12项研究的基线PaO2/FiO2比值处于中度ARDS水平(1项研究均值低至70 mmHg)。1项研究纳入接受体外膜肺氧合(ECMO)治疗的患者。体重指数(BMI)分布显示:2项研究为正常范围,6项为超重,5项为肥胖。所有患者均接受镇静及神经肌肉阻滞治疗,潮气量设置存在差异:10项研究采用6-8 mL/kg预测体重(PBW),2项为4-6 mL/kg PBW,1项为3-4 mL/kg PBW(表1)。
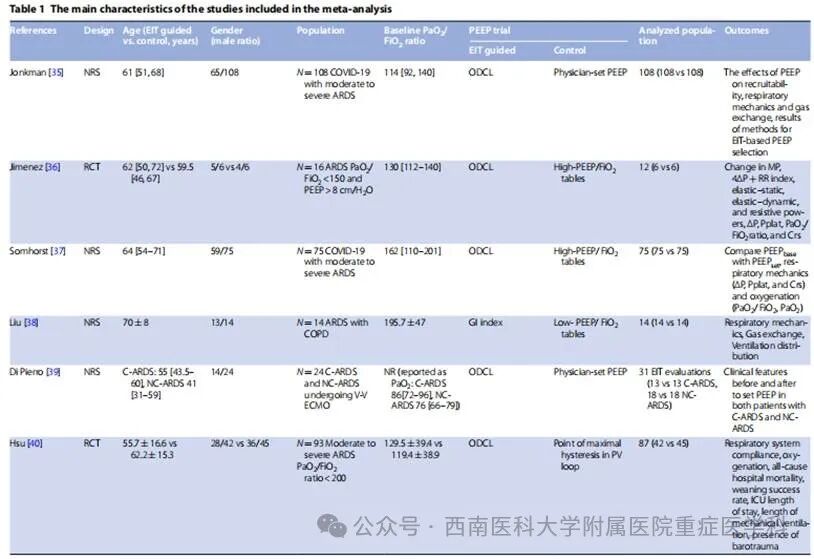
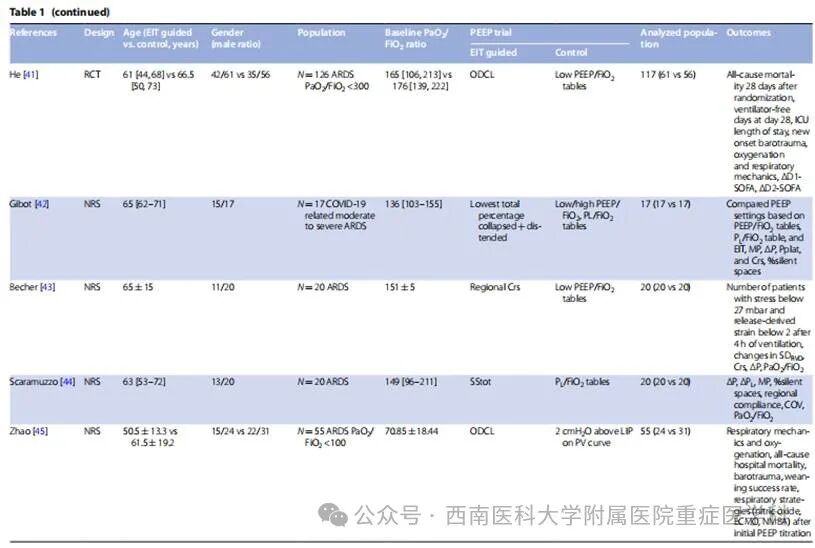
在所纳入试验的对照组中,7项研究使用PEEP/FiO2表滴定PEEP,2项研究使用PV曲线滴定PEEP;2项研究使用呼气末经肺滑动表滴定PEEP;3项研究使用医生设定的PEEP或临床PEEP。
在干预组中,PEEP滴定以EIT为指导。8项研究使用了Costa等人的累积塌陷和过度扩张百分比曲线的截点来指导PEEP滴定,而其余5项研究则使用了各种技术,包括塌陷和扩张的总百分比、全域不均一性(GI)指数、区域顺应性和呼气末肺阻抗(EELI)技术。7项研究在PEEP滴定前进行了肺复张工作,而其余6项研究没有。在9项研究中,EIT带放置在4-5肋间,在1项研究中,放置在5-6肋间,而在3项研究中没有报告。9项研究中所有患者都处于仰卧位。
纳入研究的偏倚风险
总体偏倚风险值得关注,主要潜在偏倚源于混杂因素。
主要结局指标
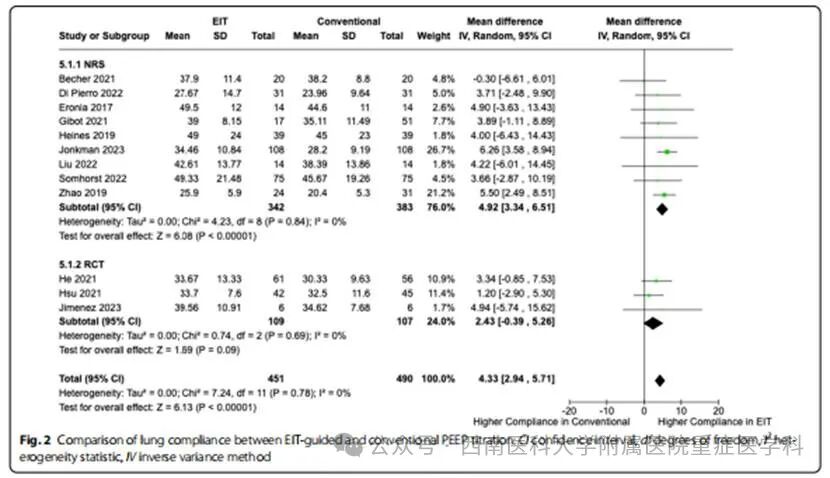
肺顺应性:12项研究(n=941)显示,EIT组较传统方法显著提升肺顺应性(MD=4.33,95% CI [2.94, 5.71],P<0.00001,I²=0%)(图2)。机械功与驱动压:EIT组机械功显著降低(n=148,MD=−1.99,95% CI [−3.51, −0.47],P=0.01,I²=0%),驱动压亦下降(n=903,MD=−1.20,95% CI [−2.33, −0.07],P=0.04,I²=89%)(图3、图4)。PEEP与平台压:两组间差异无统计学意义,但存在显著异质性。
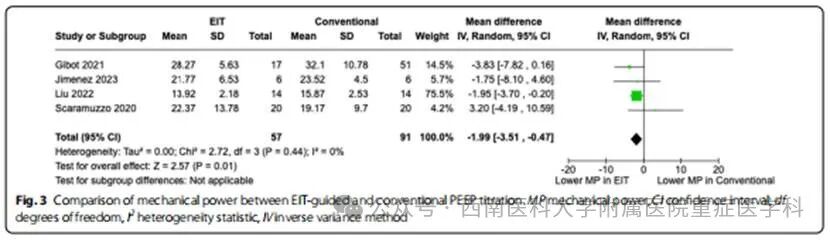
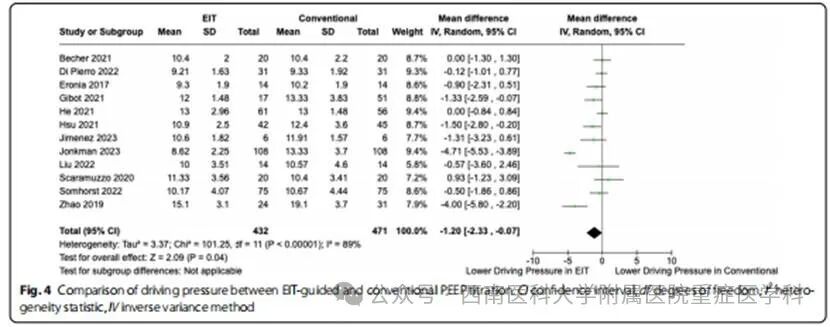
次要结局指标
三项研究(n=259名患者)提供了死亡率数据。包含62名患者死亡的两项研究(n=142)全因医院死亡率荟萃分析,显示合并相对风险(RR)为0.59(95%置信区间[0.39,0.89],P=0.01,I2=0%)。包含28例死亡的一项研究(n=117)报告了28天内的全因死亡,其RR为0.80(95%置信区间[0.42,1.52],P=0.49)。事后,包括259名患者和90名死亡患者在内的长期死亡率(两种结果的综合总体效应估计)的汇总显示,RR为0.64,95%CI[0.4,0.91],P=0.01,I2=0%。在这三项研究中,发现了肺顺应性改善的趋势,其中一项研究显示了显著改善。关于驱动压,两项研究表明显著降低,而一项研究无明显差异。EIT引导(与常规)PEEP滴定显著降低了沉默肺区的百分比。(MD=-5.23,95%置信区间[-8.72,-1.74],P=0.003,I2=5%)。然而,EIT引导的PEEP对PaO2/FiO2比值、ICU住院时间和COV百分比的影响与传统方法没有显著差异,在森林图中观察到异质性。一项研究报告了 28天的无呼吸机天数和通气持续时间,组间差异不显著。
敏感性及亚组分析
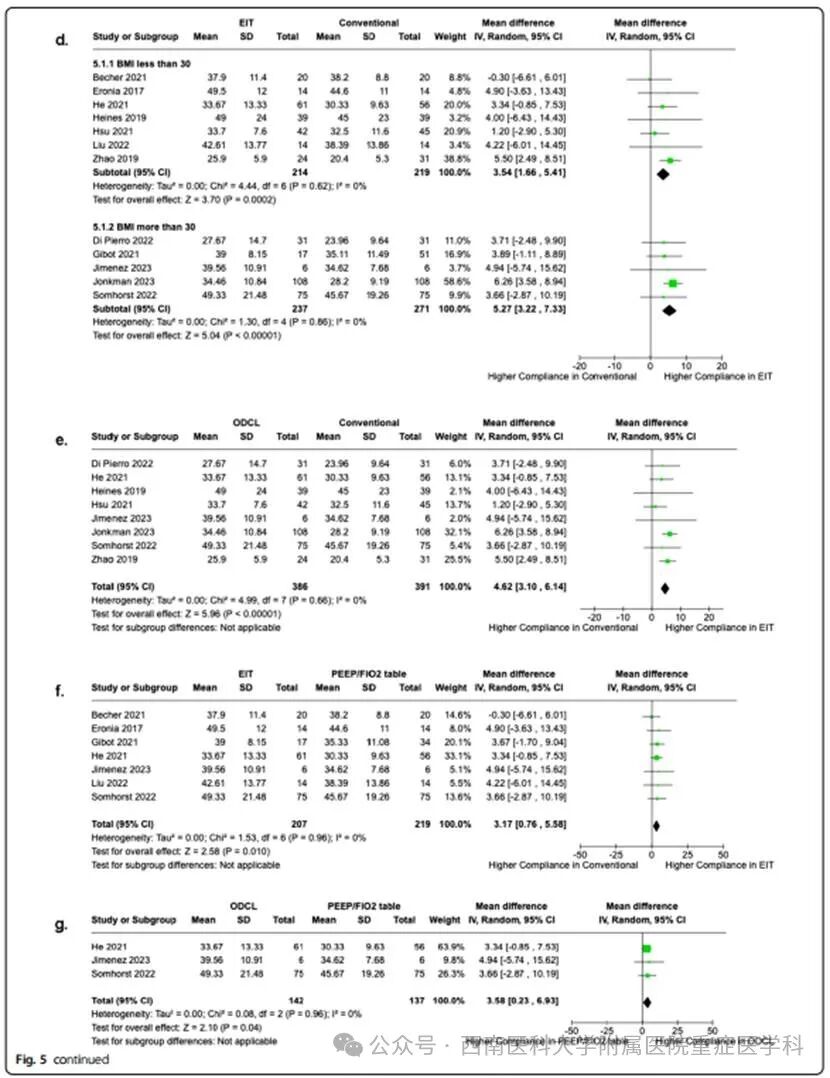
随机对照试验(vs NRS)的敏感性分析一致表明,EIT引导的PEEP对肺顺应性改善有积极作用。合并(MD)为2.43(95%CI−0.39至5.26),表明有改善的趋势,但估计值存在一些不确定性(图2)。为了进一步评估这些发现的稳健性,进行了额外的分析:排除具有高偏倚风险的研究,证实了治疗效果的一致性(M D = 4 . 0 1,9 5 % C I [ 2 . 4 5 , 5 . 5 7 ] ,P<0.00001,I2=0%),增强了结果的可靠性(图5a);在PEEP试验之前,通过排除肺复张策略的研究,将EIT引导的PEEP的影响与潜在的混杂因素隔离开来,仍显示出积极的趋势(MD=3.85,95% CI[ 1.95,5.75],P<0.0001 ,I2=0%),从而加强了EIT指导的PEEP对肺顺应性的直接影响(图5b);去除具有显著积极治疗效果的研究表明,总体积极趋势不仅仅是由少数异常研究驱动的,因为对肺顺应性的影响始终是积极的,具有统计学意义( MD=2.86 ,95%CI[0.95,4.78] ,P=0.003 ,I2=0%)(图5c)。我们对肥胖患者亚组进行了敏感性分析,以检验EIT引导的PEEP可能对这一特定亚组特别有利的假设,因为他们有不同的呼吸问题,如肺水肿、非均一通气和VILI风险增加。然而,我们的研究结果表明,与常规PEEP方法相比, EIT引导的PEEP可以提高肥胖患者(MD=5.27,95%CI[3.22,7.33],P<0.00001,I2=0%)和非肥胖患者(MD=3.54,95%CI[1.66,5.41],P=0.0002,I2=0%)的呼吸系统顺应性(图5d)。我们进行了全面的检查,比较了不同的PEEP滴定策略:ODCL法与传统方法,EIT引导的PEEP与ARDSNet PEEP/FiO2表,ODCL法和ARDSNet PEEP/FiO2表。在将ODCL方法与常规方法进行比较时,我们观察到肺顺应性的MD为4.62(95%CI[3.10 ,6.14],P<0.00001,I2=0%)(图5e)。同样,当将EIT引导的PEEP与ARDS Net PEEP/FiO2表进行比较时,MD为3.17(95%CI[0.76,5.58],P=0.01,I2= 0% )(图5f)。
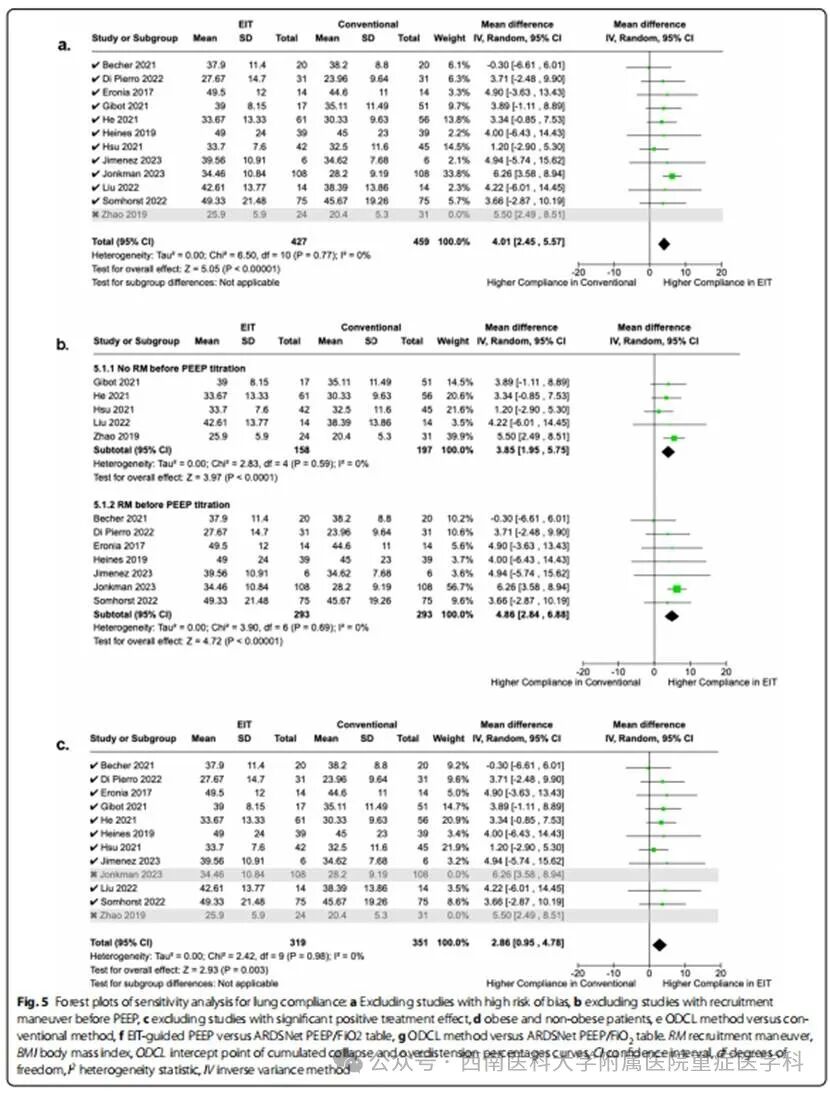
最后,ODCL法和ARDS Net PEEP/FiO2表之间的比较得出MD为3.58(95%CI[0.23,6.93],P=0.04,I2=0%)(图5g)。这些分析及其各自的统计指标突显了不同方法的肺顺应性结果的一致趋势,证明了我们研究结果的稳健性和一致性。此外,我们通过排除具有高偏倚风险的研究和使用小于6ml/kg的潮气量的研究,对DP进行了敏感性分析。排除高偏倚风险研究后,MD变为-0.9 6(95 %可信区间 [-2 .12,0.19 ],P=0.10,I2=89%),在删除使用小于6ml/kg的潮气量的研究后,统计数据变为MD−0.82 ( 95%CI[-1.63 ,-0.02],P=0.04,I2 =61%)。对于DP,在ARDS的严重程度、PEEP的增加/减少和常规干预方面观察到统计学上显著的亚组效应。关于PEEP,在ARDS的病因、ARDS的严重程度、PEEP试验前的肺复张策略以及常规和EIT干预措施方面观察到统计学上显著的亚组效应。对于PaO2 /FiO2比值,在PEEP试验和EIT干预前的肺复张中观察到统计学上显著的亚组效应。尽管如此,协变量在亚组之间分布不均,表明亚组分析可能不会产生有效的结果。然而,在有和没有肺复张的情况下,EIT(与常规)引导的PEEP在PaO2 /FiO2比值上的比较并不涉及协变量分布。虽然EIT(与常规PEEP滴定相比)的PaO2 /FiO2比值明显更高,肺复张亚组内的试验间异质性适中,导致治疗效果估计的有效性存在不确定性。
发表偏倚
Egger检验(p=0.26)及漏斗图显示无明显发表偏倚,但部分研究呈现高异质性效应值,提示结果需谨慎解读。
讨论
在本项荟萃分析中,我们发现与传统方法相比,使用电阻抗断层扫描(EIT)引导的呼气末正压(PEEP)滴定显著提高了肺顺应性,并降低了机械功率。这些效果在没有异质性的情况下观察到。此外,尽管存在显著的异质性,我们还发现驱动压力(DP)有显著降低。在纳入的13项研究(共623名患者)中,EIT引导的PEEP优化在提高肺顺应性方面表现出显著效果,这表明EIT在实时监测肺部通气分布方面具有重要价值,有助于实现个体化的PEEP调整。
EIT引导的PEEP调整在提高肺顺应性方面的效果显著,这可能归因于EIT能够实时监测肺部通气分布,从而实现更精确的PEEP调整。EIT技术能够量化肺部不均一性,分析区域和全域通气模式,并识别潜在可复张的肺区域。这些功能使得EIT在指导PEEP调整时具有显著优势,能够更好地平衡肺复张和防止过度膨胀。
此外,EIT引导的PEEP调整还显著降低了机械功率和驱动压力,这可能对减少呼吸机相关的肺损伤(VILI)具有重要意义。降低机械功率和驱动压力可能为ARDS患者带来潜在的生存优势。尽管我们没有发现EIT引导的PEEP调整对PaO2/FiO2比值、ICU停留时间和%COV有显著影响,但在三项研究中,我们观察到与肺顺应性和驱动压力改善相关的死亡率降低趋势。
我们的研究结果与近期其他研究一致,表明EIT引导的PEEP调整在ARDS患者中具有潜在的临床益处。然而,我们的研究也存在一些局限性。首先,纳入研究的患者特征和干预措施存在异质性,这可能影响结果的解释。其次,关于机械功率和驱动压力的数据有限,这限制了我们对这些结果的分析。最后,我们没有评估EIT方法的标准化,这可能影响结果的一致性和可比性。
总之,我们的系统综述和荟萃分析提供了证据,支持EIT引导的机械通气在ARDS患者中的有效性。EIT的实时肺功能评估允许个体化的PEEP设置,从而提高肺顺应性,同时降低机械功率和驱动压力。未来需要大规模的随机对照试验来验证这些发现,并特别关注死亡率、机械通气持续时间和ICU住院时间等临床结果。此外,还需要标准化EIT方法,以确保研究之间的一致性和可比性。
Intensive Care Med (2024) 50:617–631 https://doi.org/10.1007/s00134-024-07362-2
参考文献(略)
