
摘要
背景
早期控制升高的血压是急性脑出血最有前景的治疗方法。本研究旨在确定,在医院环境中实施一套以目标为导向的治疗方案(包括早期强化降压协议,以及针对高血糖、发热和异常抗凝状态的管理算法),是否能改善急性自发性脑出血患者的预后。
方法
我们在9个中低收入国家(巴西、中国、印度、墨西哥、尼日利亚、巴基斯坦、秘鲁、斯里兰卡、越南)和1个高收入国家(智利)的医院开展了一项实用性国际多中心终点设盲的阶梯式楔形集群随机对照试验。纳入标准为:医院无相关疾病特异性治疗协议或协议不统一,愿意对连续收治的(年龄≥18 岁)、发病6小时内就诊且影像学证实为自发性脑出血的患者实施该治疗方案,有本地负责人,且能提供所需研究数据。通过中心随机分配,采用置换块法将医院分为3个实施序列,分层因素为国家和12个月内预计招募的患者数量。每个序列包含4个阶段,规定医院按阶梯式方式从常规治疗对照组逐步转为治疗方案干预组,以避免干扰。在完成常规治疗对照阶段前,各医院不被告知干预措施、序列及分配阶段的详情。治疗方案包括:对存在异常的患者,早期强化降低收缩压(目标<140 mmHg)、严格控制血糖(无糖尿病者目标 6.1-7.8 mmol/L,糖尿病者目标 7.8-10.0 mmol/L)、退热治疗(目标体温≤37.5°C)、1小时内快速逆转华法林相关抗凝状态(目标国际标准化比值 < 1.5)。分析基于改良意向性治疗人群(即排除研究期间退出的机构)的可用结局数据。主要结局为6个月时的功能恢复,由设盲研究人员采用改良Rankin量表(mRS,范围0分[无症状]至6分[死亡])评估,通过比例有序 logistic回归分析mRS评分分布,并校正集群(医院)、集群每期分组及时间(2017年12月12日起的6个月周期)。该试验已在 ClinicalTrials.gov(NCT03209258)和中国临床试验注册中心(ChiCTR-IOC-17011787)注册,且已完成。
结果
2017年5月27日至2021年7月8日期间,共评估206家医院的资格,其中10个国家的144家医院同意参与并被随机分配,但22家医院在开始招募患者前退出,另有1家医院因未获得监管批准被退出,其已招募患者的数据被删除。2017年12月12日至2021年12月 31 日期间,共筛查10857例患者,排除3821例。改良意向性治疗人群共纳入121家医院的7036例患者,其中3221例分配至治疗方案组,3815 例分配至常规治疗组;治疗方案组2892例、常规治疗组3363例有主要结局数据。治疗方案组出现不良功能结局的可能性更低(共同比值比 0.86;95% 置信区间0.76-0.97;p=0.015)。在包括额外校正国家和患者变量的一系列敏感性分析中(0.84;0.73-0.97;p=0.017),以及采用不同多重插补法处理缺失数据时,治疗方案组的mRS评分均呈现一致的有利偏移。治疗方案组的严重不良事件少于常规治疗组(16.0% vs 20.1%;p=0.0098)。
引言
脑出血是最严重且最难治疗的卒中类型,约占全球每年近2000万新发卒中病例的20%[1]。大多数脑出血病例发生在中低收入国家(LMICs),这些地区高血压患病率高、饮食不健康(如高盐摄入)及存在其他危险因素[2]。由于脑出血后血压升高常见且与不良结局密切相关,患者管理的核心内容之一是将血压降至收缩压140mmHg或更低[3-7]。然而,随机对照试验结果不一致[8,9],且针对大量脑出血或需要神经外科干预患者的证据不足[10],限制了该策略在临床实践中的应用,指南对此推荐力度通常中等[3-7]。此外,由于缺乏经证实的脑出血内外科治疗方法,对这些患者的治疗缺乏紧迫性,且主动治疗的撤出阈值较低[11,12],这与现代急性缺血性卒中的治疗体系形成鲜明对比。
为提高脑出血随机对照试验识别有效治疗方法的成功率,研究人员已尝试通过临床和影像学变量定义潜在应答者群体——这些患者因持续出血或血肿扩大而极易出现早期神经功能恶化[13-15]。另一项努力是将功能结局评估延长至传统的90天之后,因为脑出血的恢复比急性缺血性卒中更长[16]。评估多种干预措施组合作为多方面治疗方案的一部分可能也具有优势,正如澳大利亚一项集群临床试验所示,实施高血糖、发热和吞咽困难的治疗方案可改善急性卒中结局[17]。英国一项单中心 “前后对照”研究进一步支持了这种方法,该研究显示,实施包括抗凝逆转、强化降压及快速分诊至神经外科和重症监护的质量改进方案,与脑出血后30天病死率降低相关[18]。国际急性脑出血强化降压试验(INTERACT2)第二阶段的事后分析[19]显示,参与者基线收缩压、血糖、体温升高及既往使用抗凝剂的评分越高,脑出血后功能结局越差。这些问题为第三次急性脑出血强化降压治疗联合干预试验(INTERACT3)的设计提供了依据,旨在确定一套以目标为导向的治疗方案(包括早期强化降压及其他异常生理指标的管理方案)是否能改善广大急性自发性脑出血患者的功能结局。
方法
研究设计
INTERACT3是一项在9个中低收入国家(巴西、中国、印度、墨西哥、尼日利亚、巴基斯坦、秘鲁、斯里兰卡、越南)和1个高收入国家(智利)的医院开展的国际多中心前瞻性阶梯式楔形集群随机终点设盲对照试验。该试验采用“探索-实施”混合设计,随着医院被随机分配在不同时间点从常规治疗对照组转为干预实施组,对患者集群进行前瞻性随访以确定结局。这种试验方法旨在模拟新质量改进政策的自然推广过程,即实施以目标为导向的强化治疗方案,包括快速纠正急性脑出血患者的任何异常生理指标(高血压、高血糖、发热)和凝血功能异常。该试验遵循阶梯式楔形集群随机试验的CONSORT扩展报告指南[20]。方案和统计分析计划的详情已在其他文献发表[21,22],详见附录(第89-221页)。
该研究已获得参与医院伦理委员会和相关监管机构的批准。采用混合consent 流程:集群监护人(适当的高级代表,如首席执行官)同意急性脑出血患者接受干预作为常规治疗的一部分。参与者(或经批准的代理人)提供书面知情同意,允许收集社会人口学、医学和临床信息,并同意在6个月时接受结局评估。2017年7月12日的原始方案有两项修订:记录额外资金来源,延长亚洲地区各干预阶段时间至4个月以最大限度招募患者,允许在进入实施阶段前有7-10天的过渡期,将分层变量纳入随机化程序,延长研究时间线(2018年4月 8日);此外,增加医院数量,进一步延长研究时间线,在试验中嵌入过程评价和经济评价,明确脑出血诊断的纳入标准,纳入记录退出研究患者consent的表格,明确各研究阶段达到所需样本量的患者招募目标(2019年8月12日)。
集群和参与者
通过神经外科和神经内科专业网络联系医院。符合条件的医院要么没有管理急性脑出血患者异常生理指标的协议,要么协议不统一,且愿意将所需的干预性治疗方案作为常规治疗的一部分实施。符合条件的机构需连续招募发病6小时内就诊的成年(年龄≥18岁)急性脑出血患者,有愿意领导干预实施的本地代表(称为负责人),且能提供所需的研究数据。主要患者排除标准包括:脑出血继发于脑部结构异常(如动静脉畸形、颅内动脉瘤、肿瘤、创伤或既往脑梗死)或再灌注治疗(如静脉溶栓或血管内取栓);或治疗医师判断患者不太可能遵守研究治疗或随访方案(或两者均不遵守)。纳入和排除标准的详细内容见附录(第14页)。
随机化和盲法
符合条件的医院由试验统计学家(李强)使用计算机生成的列表,通过置换块法随机分配至3个序列(含4个阶段),分层因素为国家和各机构研究期间预计招募的患者数量——<80、80-160 和> 160 例。在第1阶段,所有机构均对脑出血患者采用常规治疗和监测方案。分配至序列1的机构在第2阶段开始实施治疗方案,序列2在第3阶段,序列3在第4阶段,详见附录(第26-30、78页)。触发机构进入下一阶段的标准是达到预定的患者招募目标,或自每个阶段开始日期起满3个月(亚洲地区为4个月,因患者招募能力更强)。为避免干扰,在完成常规治疗对照阶段前,不向各机构透露干预措施、序列和分配阶段的详情。从常规治疗过渡到干预阶段前,有7-10天时间供机构工作人员接受培训。位于国家中心办公室(中国、智利、巴西、尼日利亚)或医院(其他国家)且对分组和患者详情设盲的训练有素的研究人员,在患者随机化后6个月通过电话评估结局。
出于后勤和资金原因,机构分批次启动,2017年始于中国,随后2019年扩展至其他国家(附录第26-32、79-80 页)。然而,由于COVID-19大流行,智利、巴基斯坦和秘鲁的患者招募在2020年3月1日至8月31日期间暂停,2020年11月2日之前,中国以外的新医院均未开始招募患者。由于大流行影响患者招募(主要是干预阶段的机构),导致随机分组的患者数量不平衡,因此延长了该阶段的持续时间,以允许尽可能多的机构参与并招募患者进入干预组。
程序
在医院开始筛查和招募患者前,参与机构的关键人员在区域和各医院会议上接受研究程序培训。在完成常规治疗对照阶段后的7-10天内,这些人员接受在线培训和远程沟通,了解适用于合格患者的强化治疗方案体系。治疗方案包括:早期强化血压管理,目标是在治疗开始后1小时内将收缩压降至140 mmHg以下,130 mmHg为停止治疗的阈值;强化控制升高的血糖,目标是治疗开始后尽快达到无糖尿病者6.1-7.8mmol/L、糖尿病者7.8-10.0 mmol/L 的血糖目标,这是指南推荐的低血糖风险最低的目标[23];发热治疗,目标是开始治疗后1小时内将体温降至37.5°C以下;对服用华法林者,使用新鲜冰冻血浆或凝血酶原复合物纠正异常抗凝状态,目标是治疗后1小时内国际标准化比值 < 1.5。护理方案中的所有目标浓度需在患者中维持7天(或直至出院或死亡,以先发生者为准)。上传至研究数据库的各机构血压、血糖、体温和国际标准化比值数据,用于检查方案依从性,并允许试验人员向机构提供反馈和进一步培训。所有机构每月收到绩效报告,且要求工作人员至少参加两次研究期间反复举行的在线质量改进会议。过程评价通过在试验期间进行形成性利益相关者参与访谈,深入了解改变治疗体系和实施方案的障碍与促进因素[24]。该信息也为机构工作人员将治疗方案整合到实践中的培训提供了进一步指导。治疗方案的详细内容见附录(第88-170 页)。
为确保持续招募,每个参与机构需将所有诊断为脑出血的患者登记到筛查和入组日志中。对于入组患者,入院时收集人口统计学和临床数据,包括使用美国国立卫生研究院卒中量表(NIHSS,范围0-42,分数越高表示神经功能缺损越严重)测量的神经功能损害程度。医院工作人员在治疗第1天和第7天(或更早出院或死亡时)收集临床状态、管理和结局的随访数据,独立工作人员在6个月时收集结局数据。1619例患者(每个机构常规治疗和干预阶段的前7例患者)在就诊时(诊断扫描)、治疗24小时和7天时的脑部影像上传至安全的中央影像服务器,由对治疗分配设盲的训练有素的医师进行分析。集中判定的脑部影像结果将在未来的出版物中呈现。
结局
主要结局是6个月时采用改良Rankin量表(mRS)测量的功能恢复,并作为有序结局(所有类别间的偏移)进行分析。mRS是一种标准的全球失能测量工具,评分从0到6,其中0-1分表示结局良好(无症状或有症状但无失能);2-5分表示失能程度逐渐增加(及依赖性);6分表示死亡。次要结局包括6个月时mRS评分的二分法分析:3-6分(失能或死亡)vs 0-2分,以及存活者中3-5 分(严重失能)vs 0-2分;6个月时死亡;7天时根据NIHSS评分变化的死亡或神经功能恶化(既作为连续测量,也分为7组:<5、5-9、10-14、15-19、20-24、≥25 和死亡)[25];使用欧洲生活质量5维度自评问卷(EQ-5D-3L)测量的健康相关生活质量;以及6个月时的居住地(自己家vs其他地方)。出院时间也进行了计划,但仅在第7天进行了记录,以配合此时进行的其他评估,因此以第7天为截止日期。随访期间根据标准定义记录全因和特定原因严重不良事件的安全性结局。
统计分析
本研究设计的检验效能为90%(α=0.05),采用有序logistic回归检测6个月时不良功能结局的共同比值比(OR)为0.8。该设计需要110个机构的8360例患者,假设常规治疗组的mRS 评分分布与INTERACT2研究中接受标准低强度降压治疗的对照组相似[26],且5% 的患者失访。与常规治疗相比,接受集束化治疗后,较差功能结局(改良Rankin量表评分3~6)的发生率下降了5.6%,从55.6%降至50.0%。基于INTERACT2和另一项国际急性卒中集群随机试验的结果,我们假设组内相关系数为0.04[25]。所需样本量(每个参与医院每个阶段平均招募19例患者,即110个机构×4个阶段×19例患者)使用PASS软件2019计算,通过对两个有序分类变量的检验[27],并根据阶梯式楔形设计对集群进行调整[28]。
所有分析均在患者水平进行,并校正集群效应。主要分析基于改良意向性治疗,纳入所有提供书面同意且有主要结局数据的参与者,无论是否遵守方案。主要分析采用有序logistic 回归,包含集群(医院)的随机效应、时间(4个阶段)的固定分类效应,以及每个集群每期分组的固定效应。然而,在揭盲数据后,我们发现该试验不符合所有集群同时从一个阶段过渡到下一个阶段的标准阶梯式楔形设计[29],因为阶段长度不等,且不同集群从对照转为干预的时间差异很大(附录第26-30、78-79页)。为更恰当地说明时间效应,我们使用6个月日历周期代替试验阶段来校正日历时间,这与从第一名患者招募(2017年12月12日)到最后一名患者招募(2021年12月31日)期间个体患者临床结局评估的随访时间长度一致(附录第32页)[30,31]。
我们进行了一系列预先计划的敏感性分析,采用各种缺失值插补方法[22]、跨机构的可变时间效应[32],以及在主要模型中额外校正国家(按地区分组:中国 vs 印度、巴基斯坦、斯里兰卡、越南 vs 巴西、秘鲁、智利、墨西哥、尼日利亚)、卒中前功能(估计的mRS分类评分0-5)、年龄、性别和基线NIHSS评分等协变量。NIHSS评分也作为连续变量,采用假设正态分布和恒等链接函数的未校正分层线性回归模型进行分析。我们还通过基于1个月和3个月日历时间窗口的限制性立方样条对时间效应进行连续建模,进行事后敏感性分析。
我们发现违反了比例优势假设,但基于治疗效应在mRS各类别间不恒定的理解仍继续进行分析。通过条形图的类别间偏移图形评估以及二元分析对结果进行补充。按计划,分析的6个亚组为年龄、性别、国家、NIHSS 评分(<15 vs≥15),以及研究者报告的基线血肿体积(<15 mL vs15-<30 mL vs≥30 mL)和位置(皮质vs深部vs脑干、小脑或原发性脑室),并检验特定亚组与主要结局治疗效应之间的交互作用。事后估计治疗获益所需的治疗人数,以帮助解释结果。
尽管研究期间进行了两次中期分析,但由于采用保守的Haybittle-Peto停止规则[33],且I类错误率消耗极少,主要结局(包括敏感性分析)的显著性阈值仍为p<0.05。对于7项次要临床结局,我们通过应用序贯Holm-Sidak校正[34]控制家族误差率,以方便解释研究结果[35]。采用重复测量线性混合模型评估干预性生理指标的组间差异,校正治疗、时间和治疗-时间交互作用的固定效应、机构的随机效应,并通过重复患者效应(假设复合对称结构)建模患者内相关性。我们使用SAS Enterprise Guide(8.2版)和R(4.0.0 版或更新版本)进行统计分析。该试验已在ClinicalTrials.gov(NCT03209258)和中国临床试验注册中心(ChiCTR-IOC-17011787)注册。
结果
2017年5月27日至2021年7月8日期间,共评估206家医院的资格,其中10个国家的144家医院同意参与并被随机分配,但22家医院在招募患者前退出。在剩余的122家医院中,43家被随机分配至序列1,37家至序列2,42家至序列3。出于后勤原因,机构分四批随机分配。前三批(每批30个机构)针对中国的机构,每批持续3-4个月;第一批为2017 年11月17日至2019年9月16日;第二批为2018年4月20日至2019年6月25日;第三批为2018年8月29日至2019年11月2日。第四批的随机分配(包括2020年4月16日至 11月25日的6个中国机构,以及所有中国以外的机构)在2019年3月20日至2021年3月31日期间进行。分配至序列3的1家医院在实施干预后因未获得必要的监管批准而被退出,其数据被删除。由于COVID-19的影响(32个机构)、无合格患者(17个机构)、负责人离开医院后失去兴趣(11个机构)、监管变化(2个机构)和提前达到招募目标(2个机构),医院在各阶段的参与率趋于下降(附录第26-30页)。即便如此,入组患者数量在随机序列和各阶段间保持平衡(图1;附录第31页)。2017年12月12日至2021年12月31日期间,共筛查10857例急性脑出血患者,3821例被视为不合格,最常见原因是发病至就诊时间超过6小时。7036例患者被随机分配至试验,其中3815例分配至常规护理组,3221例分配至治疗方案干预组。阶梯式楔形研究时间线、各序列和阶段招募的患者数量,以及患者排除原因见附录(第33页)。常规治疗组374例(9.8%)和治疗方案组222例(6.9%)患者失访,另有常规治疗组78例(2.0%)和治疗方案组107例(3.3%)患者在最后一次访视时的mRS功能状态缺失。因此,常规治疗组3363例和治疗方案组2892例患者有主要结局数据,被纳入主要疗效分析(图1)。主要结局数据的参与者比例和评估方法在组间和各阶段间保持平衡(附录第31、34-35页)。
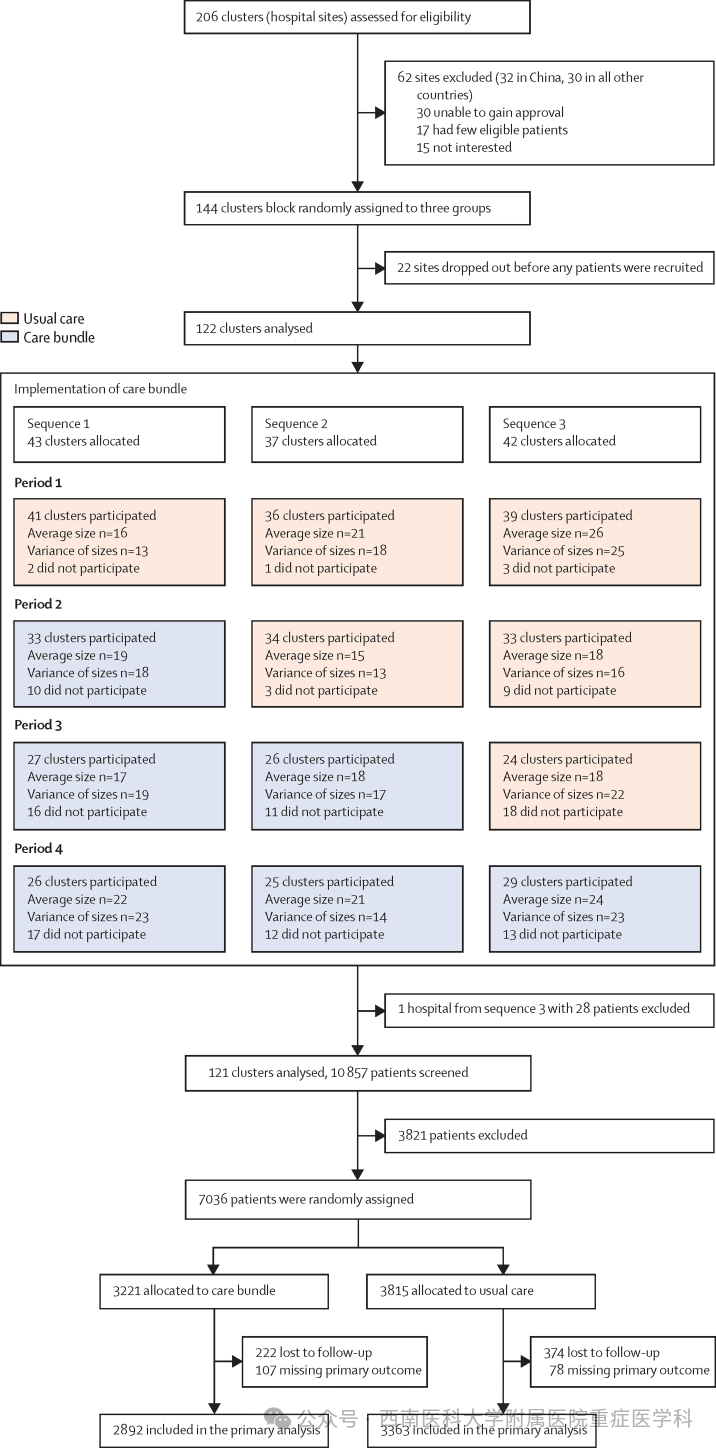
图1
患者的基线人口统计学、病史以及临床和脑部影像特征在治疗组间保持平衡(表1;附录第36页)。
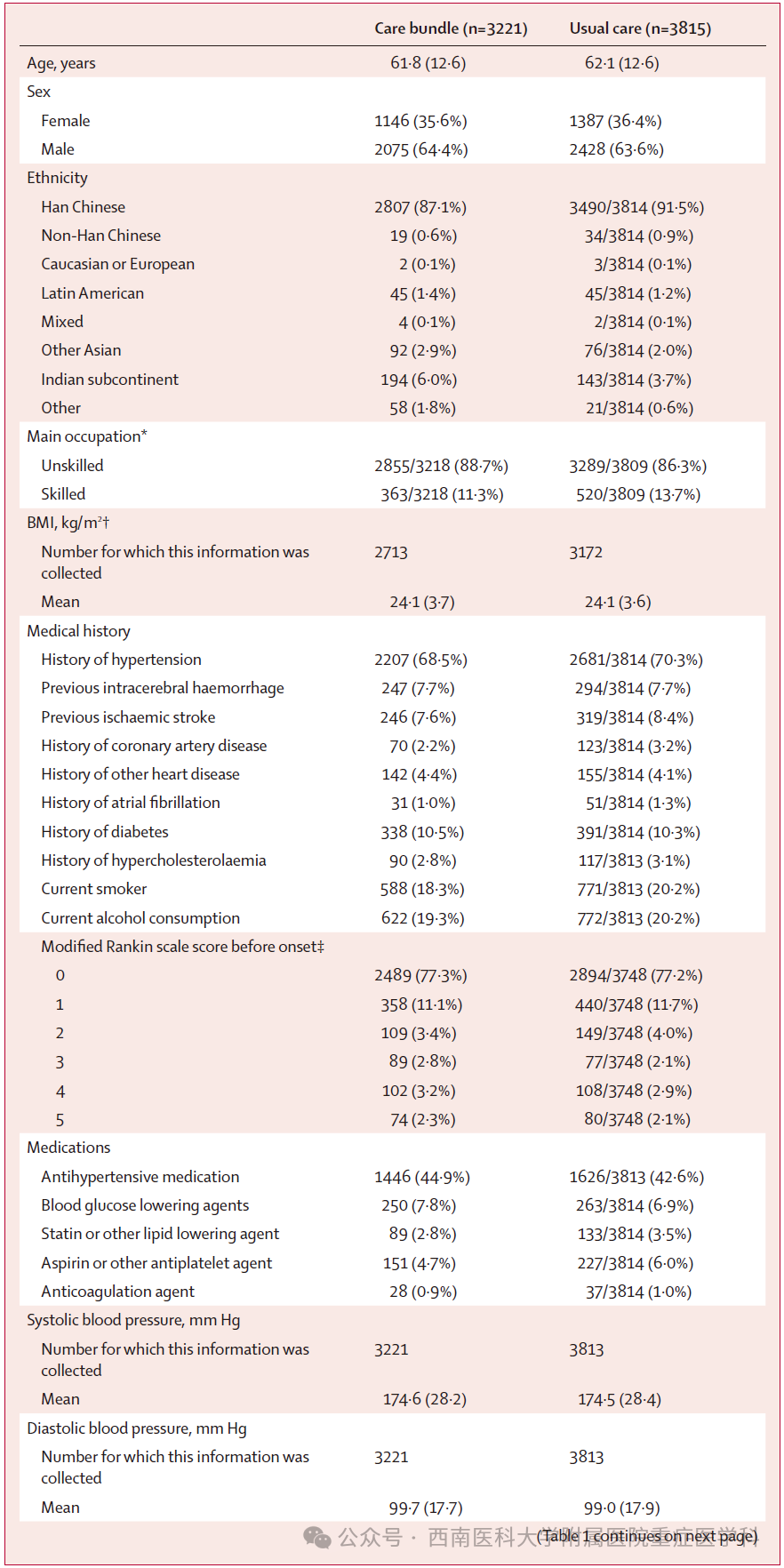
表1
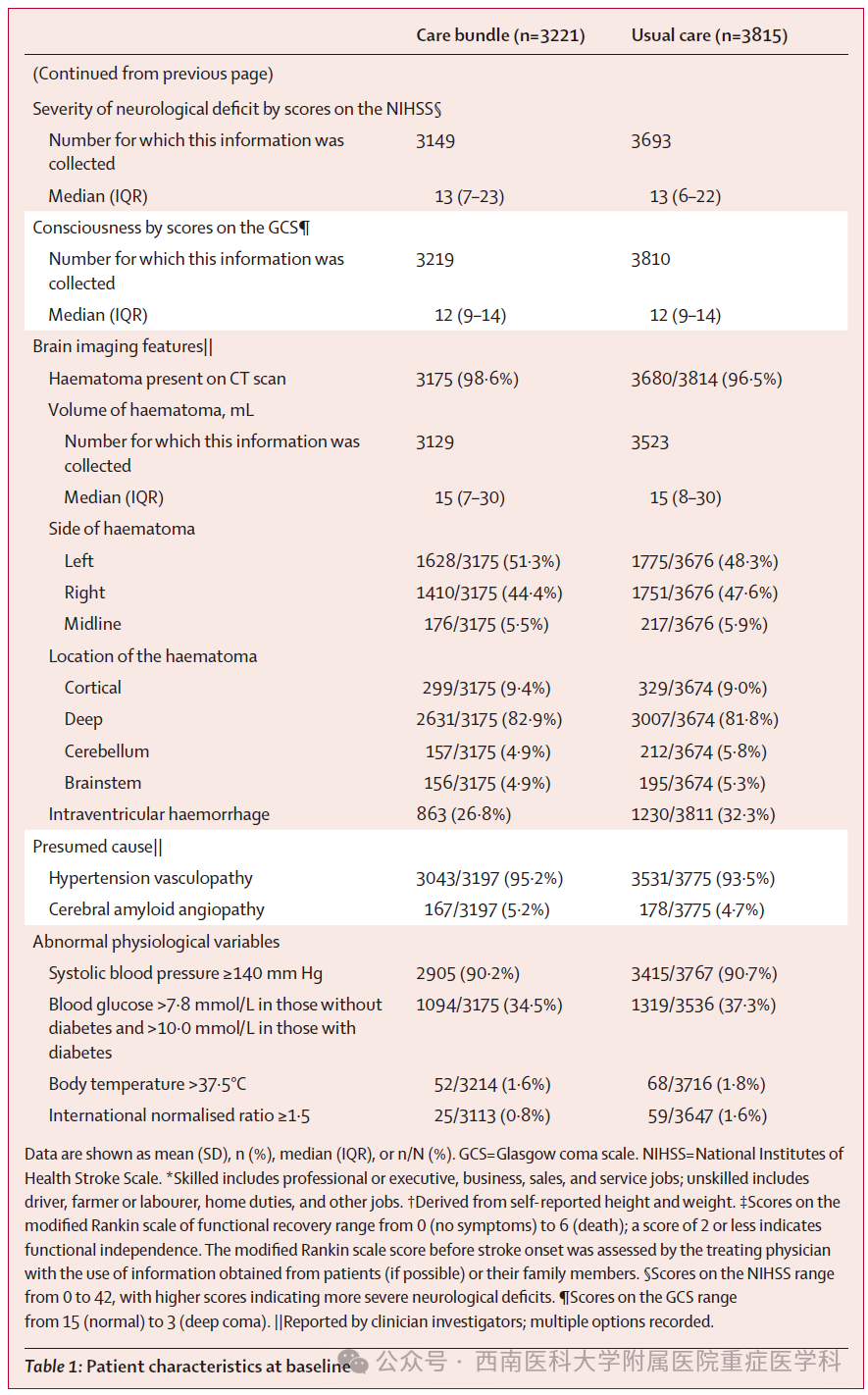
表1-续表
平均年龄为62.0(SD 12.6)岁,7036例患者中2533例(36.0%)为女性,6350 例(90.3%)为中国人。格拉斯哥昏迷量表中位评分为12(IQR 9-14),NIHSS中位评分为13(IQR 7-22)。6972例患者中6574例(94.3%)的脑出血原因推测与高血压相关,6849例患者中5638例(82.3%)的出血部位位于大脑半球深部(附录第37页)。6652例患者的中位血肿体积为15.0 mL(IQR 7.8-30.0),7032例患者中2093例(29.8%)存在脑室出血。7035例患者中5160 例(73.3%)直接收入神经外科,6988例患者中6320例(90.4%)的血压≥140 mm Hg,总体平均收缩压为174.5 mm Hg(SD 28.3)。6711例患者中2413例(36.0%)血糖升高,总体平均血糖浓度为8.0 mmol/L(SD 2.9)。6930例患者中仅120例(1.7%)体温升高,6760例患者中84例(1.2%)就诊时国际标准化比值升高。
治疗方案组前24小时接受任何静脉降压药物的患者比例高于常规治疗组(3221例中 2542例[78.9%] vs 3811例中2703例[70.9%]);第2-7天结果相似(治疗方案组3188例中2131 例[66.8%] vs常规治疗组3775例中2277例[60.3%];表2;附录第38-39页)。前24小时最常用的静脉药物为乌拉地尔(3351例[61.2%])、硝普钠(1169例[21.4%])、拉贝洛尔(663例 [12.1%])、尼卡地平438例[8.0%])和尼莫地平432 例 [7.9%]),5473例接受降压治疗的患者有记录(附录第38页)。治疗方案组1小时时平均收缩压为148.4 mm Hg(SD 21.5),24 小时时为 136.1 mm Hg(16.5);常规治疗组1小时时为154.7 mm Hg(22.5),24小时时为139.0 mm Hg(17.2)(24 小时校正平均差为-3.6 mmHg;95% 置信区间- 4.5至-2.7;p<0.0001;图2A)。治疗方案组达到收缩压≤140 mm Hg 目标的速度快于常规治疗组(中位时间2.3小时[IQR 0.8-8.0] vs 4.0小时[1.9-16.0];表2)。
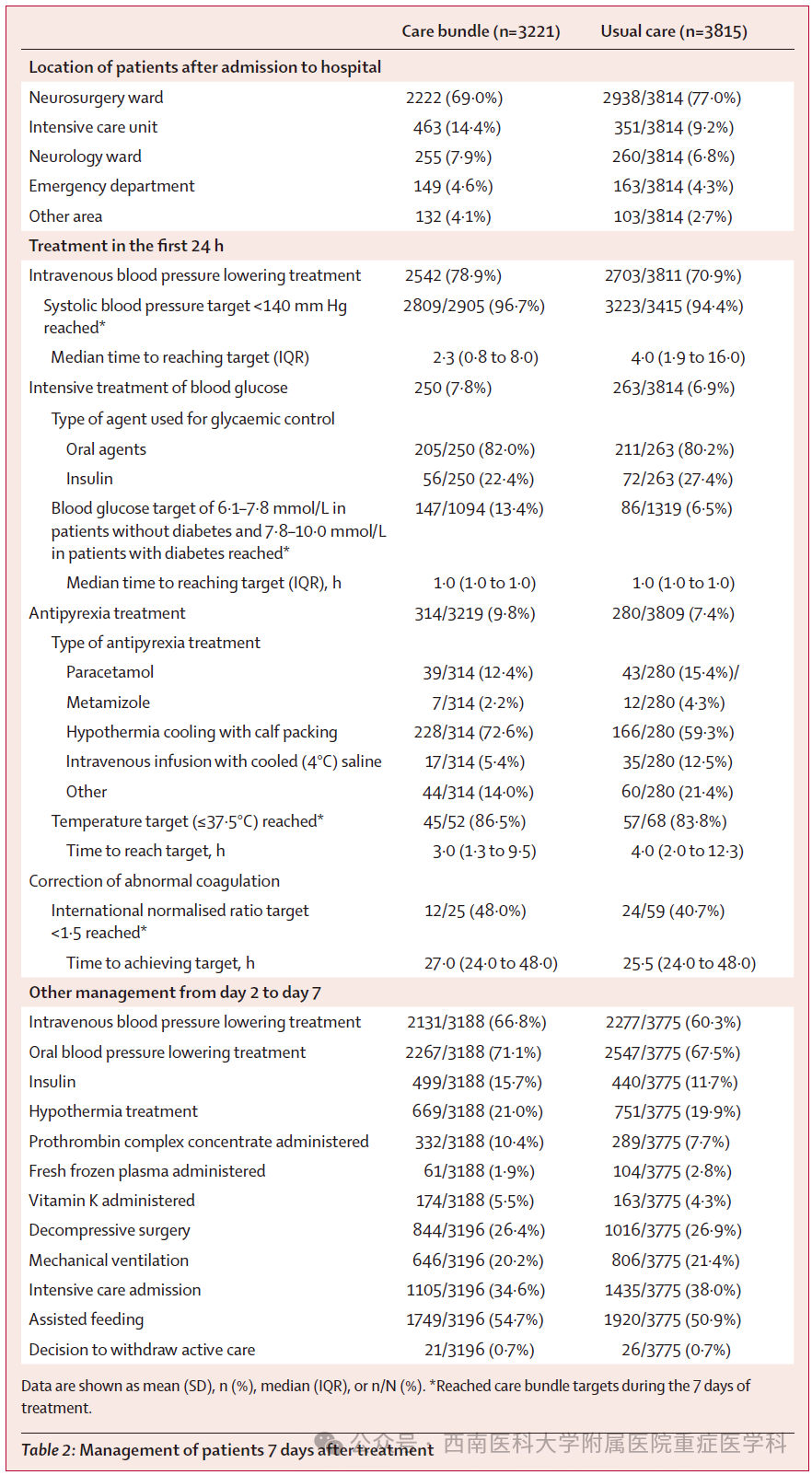
表2
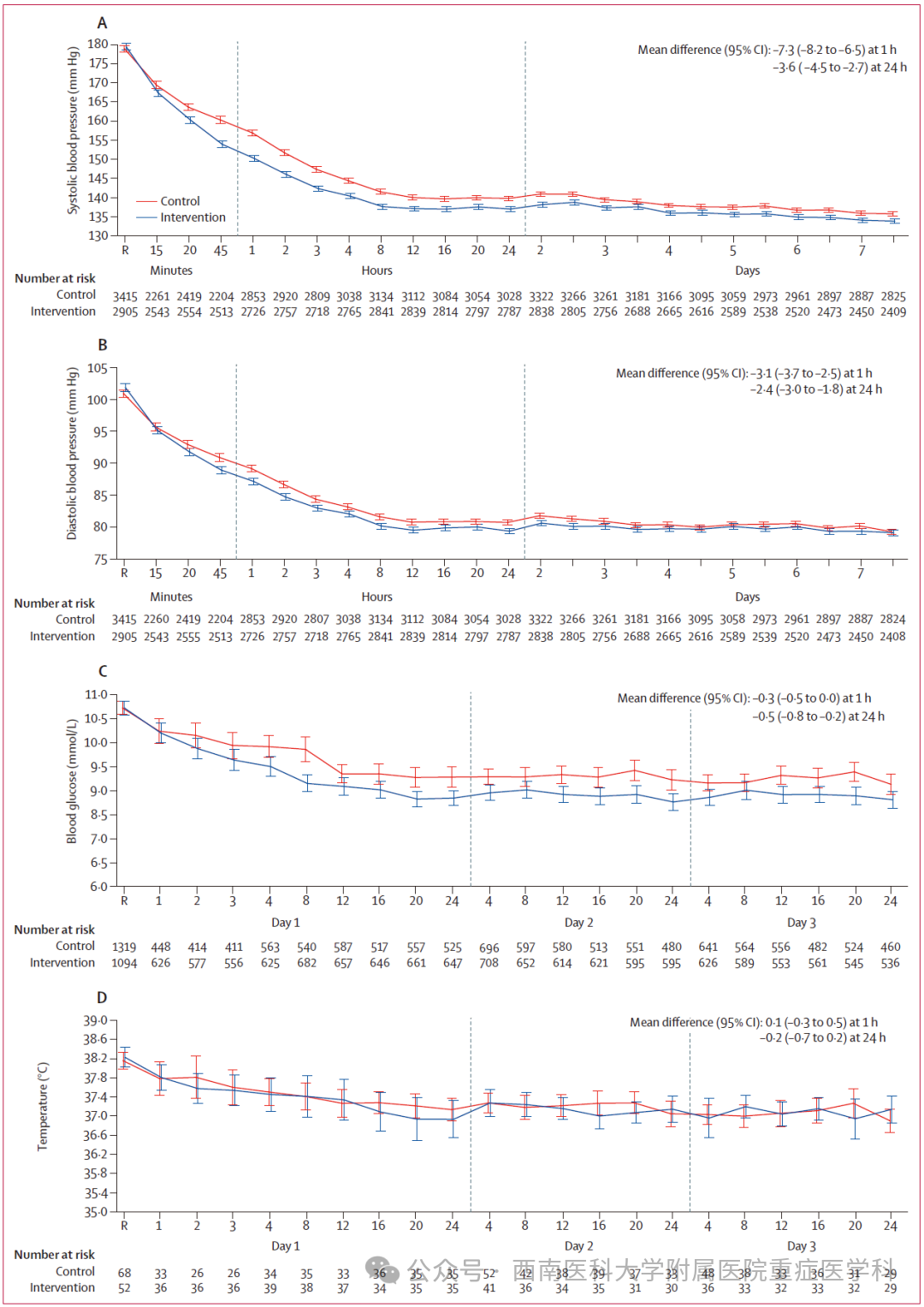
图2
治疗方案组1小时时平均舒张压为86.2 mmHgSD 13.8),24小时时为78.9 mmHg(11.5);常规治疗组1小时为88.3 mmHg(14.2),24小时为80.4 mmHg(12.1)(24小时校正平均差为-2.4 mm Hg;95% 置信区间-3.0至-1.8;p<0.0001;图2B)。治疗方案组达到血糖目标控制的患者比例高于常规治疗组(1094例中147例[13.4%] vs 1319例中86例[6.5%]),尽管 24小时校正平均血糖浓度差异微小(-0.5 mmol/L;95%置信区间-0.8至-0.2;图2C),且达到血糖控制目标的时间(中位时间1.0小时[IQR 1.0-1.0] vs 1.0小时[1.0-1.0])也无差异。治疗方案组发热患者的体温控制频率也高于常规治疗组(52例中45例[86.5%],中位时间3.0小时 [IQR 1.3-9.5] vs 68例中57例[83.8%],中位时间4.0小时[2.0-12.3]),但两组24小时总体校正平均差异无统计学意义图2D)。抗凝逆转方面无明显差异(治疗方案组25例中12 例[48.0%],中位时间27小时[IQR 24.0-48.0];常规治疗组59例中24例[40.7%],中位时间25.5小时[IQR 24.0-48.0])。表3(及附录第40页)显示,7天内其他管理方法无主要差异,尤其是去骨瓣减压术、气管插管和早期停止治疗的应用。血肿体积和NIHSS评分随时间的分布见附录(第80-81页)。
治疗方案组患者的mRS评分优于常规治疗组,所有mRS的平均效应共同OR为0.86(95%置信区间0.76-0.97;p=0.015),比例优势假设检验显示违反(p=0.0003;图3;附录第41-43页)。采用预先指定的插补方法替代缺失数据后,治疗方案组的mRS评分仍呈现有利偏移,但极端评分6分(死亡)除外(附录第44-46页)。进一步校正国家和患者特征后(表3),以及采用不同时间趋势时,这些偏移仍具有统计学意义(附录第46页)。此外,结果与采用限制性立方样条变量对时间进行建模的事后分析一致(附录第52页)。当按照最初计划使用研究阶段而非日历时间对时间进行建模时,无论是否校正或是否采用不同时间趋势,随机组间均无明显差异(附录第52-54页)。
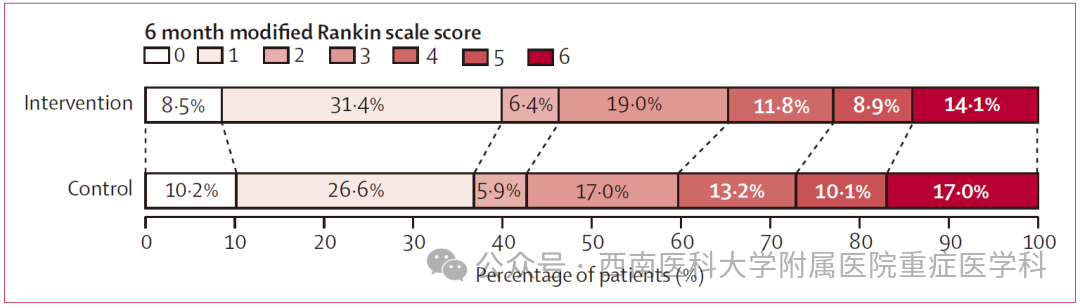
图3
次要结局结果一致,所有点估计均有利于治疗方案组,包括死亡率、健康相关生活质量和出院时间的显著差异(表3;附录第46-48页)。与常规治疗组相比,主要模型中治疗方案组6个月内死亡的比值更低(共同OR 0.77;95%置信区间0.63-0.95;p=0.015;附录第82页)。校正国家和患者特征后,差异无统计学意义(0.84;0.65-1.07;p=0.16)。90天时死亡或失能(mRS评分3-6分,54% vs 57%;0.89;0.78-1.02;p=0.10)或7天时死亡或神经功能恶化(0.89;0.77-1.03;p=0.12)的比值无显著差异。随机组间健康相关生活质量存在一些差异,包括治疗方案组的总体效用评分高于常规治疗组(平均差异0.04,95% 置信区间0.02-0.07;p=0.0008;表3),但进一步校正后这些差异减小。治疗方案组第7天前出院的患者比例显著较低(OR 0.72,95%置信区间0.53-0.98;p=0.034),但6个月时的居住地无差异。在多重检验的家族误差控制后,7项次要结局中仅EQ-5D-3L效用评分在治疗方案组显著更高(附录第54页)。
基于地区和COVID-19时期的亚组中,主要结局的治疗效应存在显著异质性(附录第 55-61、83页),这些变量相关,因为所有非中国机构均在COVID-19大流行后启动。中国机构的治疗效应在COVID-19前后无异质性(附录第84页)。在印度、巴基斯坦、斯里兰卡和越南这一国家分组中,患者达到目标收缩压的组间差异大于中国和其他国家分组(巴西、秘鲁、智利、墨西哥、尼日利亚;附录第85-87页)。然而,在其他管理方面,包括去骨瓣减压术(中国治疗方案组 vs 常规治疗组:29.5% vs 28.8%;印度、巴基斯坦、斯里兰卡、越南:2.1% vs 2.3%;巴西、秘鲁、智利、墨西哥、尼日利亚:7.2% vs 7.6%)和重症监护(中国:10.9% vs 8.4%;印度、巴基斯坦、斯里兰卡、越南:9.2% vs 6.6%;巴西、秘鲁、智利、墨西哥、尼日利亚:9.3% vs 15.2%),中国与各分组地区的随机组间无主要差异(附录第62-64页)。
总体而言,治疗方案组的严重不良事件显著少于常规治疗组(3221例中516例 [16.0%] vs 3815例中767例[20.1%];p=0.0098)。严重不良事件和死亡原因的完整列表见附录(第 65-72页),死亡原因详情见附录(第73-76页)。根据主要模型,校正后频率显示,治疗方案组54.1%(原始数据1553/2892例[53.7%])和常规治疗组56.9%(1927/3363例[57.3%])的患者估计出现死亡或严重失能,治疗方案组11.4%(407/2999例[13.6%])和常规治疗组 14.3%(571/3441例[16.6%])的患者估计出现死亡。因此,治疗方案预防1例患者发生死亡或严重失能所需治疗人数估计为35(95% 置信区间15 至无穷大),预防1例患者死亡所需治疗人数也为35(17至无穷大)。
讨论
这项在不同医疗环境中进行的实用性阶梯式楔形集群随机对照试验表明,对于发病 6 小时内就诊的急性脑出血患者,采用包括早期控制升高的血压以及高血糖、发热和异常凝血管理算法的护理方案,可改善6个月时的功能结局。这一阳性结果在一系列敏感性分析和次要结局中保持一致。
与常规治疗相比,实施时间敏感的治疗方案还与患者随访期间的生存率提高、健康相关生活质量改善和严重不良事件减少相关。鉴于118家参与医院每年收治的急性脑出血患者均超过100例,这种有益效应的规模相当于每个机构每年至少有若干类似患者的结局得到改善。
据我们所知,这是第一项显示急性脑出血急性治疗阳性结局的3期多中心随机对照试验,也是少数在多个国家采用阶梯式楔形集群随机设计的试验之一[36]。脑出血试验因干预启动的最佳时机、结局评估以及控制入组时已存在或随访期间因干预或患者病情出现的合并症混淆因素等方面的不确定性而变得复杂[13,14,16]。以往急性脑出血早期强化降压试验结果喜忧参半,原因是降压方法不同且样本量小。个体患者数据荟萃分析通过增加样本量、纳入更广泛的患者以及校正基线预后变量不平衡,增强了治疗效应的可靠性,结果显示谨慎、有针对性且持续地降低收缩压是安全的,并与脑出血后更好的功能结局相关[8,9]。然而,由于这些数据来自具有严格纳入和排除标准的传统试验,结果仅限于根据标准临床和影像标准判断预后较好、病情轻至中度的脑出血患者。我们假设将早期降压治疗与其他简单医疗干预相结合,可能在脑出血中产生叠加益处。这种多方面方法得到“急性卒中治疗质量试验”的支持,该试验中,2005至2010年在澳大利亚19个急性卒中单元实施护士主导的发热、高血糖和吞咽困难管理协议后,急性卒中患者的结局得到改善[17]。此外,英国一家大型医院实施包括抗凝逆转、强化降压及快速分诊至神经外科和重症监护的质量改进协议,提高了急性脑出血患者的生存率[18]。
然而,实施的保真度与干预效果之间可能存在复杂关系。强化降压是治疗方案的核心组成部分,因为其有强有力的证据支持,适用于多种环境,且具有合理的作用机制——减轻脑出血增长可减少脑组织剥离和压迫的原发性损伤。尽管本研究向研究者强调在早期6小时纳入时间窗内快速控制血压,但大多数脑出血增长发生在症状出现后几小时内[37]。此外,降压治疗对这一中间终点的效应温和,且至今未明确其时间依赖性关联[9]。早期纠正异常抗凝状态可能通过类似机制使患者获益[38],但与高收入国家老龄化人群因房颤和其他心血管疾病广泛使用抗血栓药物不同,本研究人群中仅少数患者为抗凝相关脑出血。红细胞和血液产物分解引起的神经炎症是脑出血后继发性脑损伤的关键因素,发生在血肿周围区域,并持续数天至数周[39]。由于高血糖[40]和发热[41]可能加剧这一过程,对其进行治疗可能提供关键的辅助治疗策略[42]。同样,这些情况仅发生在少数参与者中,随机组间的控制程度差异小。因此,尽管总体治疗效应似乎由强化降压驱动,但对生理指标的积极多方面管理以及相关的更密集监测和护理,可能影响行为和态度(包括患者的自我管理),从而在出院后仍能带来益处。计划进行中介分析,以确定治疗方案各组成部分和卒中治疗其他关键方面对结局的影响。
本试验的优势包括对复杂干预的评估,既适用于真实世界环境中的实施,也关注临床效应,且在6个月时评估以患者为中心的可靠结局。大样本量使得能够检测到适度但仍具有临床意义的益处,且由于纳入了来自不同资源环境、种族和社会人口学多样化的人群,结果具有可推广性。广泛的纳入标准允许对脑出血患者的常规分诊和治疗进行相关测试,且分诊遵循预先指定的分诊计划。提供方案、管理算法和简短培训包,同时将个体患者管理交由治疗团队酌情处理,并辅以绩效监测,这反映了该干预可能被更广泛采用的方式。在中国已发现的实施困难[24](如担心方案规定的血压和血糖控制目标可能伤害患者,以及与人员流程和药物供应相关的背景因素是否更广泛存在),正通过我们嵌入的过程评价进行调查。鉴于对最佳实践标准化和组织良好的体系质量要求的广泛需求,以及脑出血缺乏其他明确有效的治疗方法,我们预计我们的发现也将支持在高收入国家实施和加强脑出血协议。
我们的试验存在局限性。我们选择阶梯式楔形集群随机设计,是为了在常规实践中快速招募大量患者,包括病情严重和需要紧急神经外科手术的患者,这些患者难以获得早期批准。治疗方案的引入需要改变参与患者院内流程的不同临床科室的实践。这些问题使得个体随机化不可行、不公平且容易受到干扰。然而,这种研究设计的一个重要潜在局限性是日历时间的长远趋势混淆效应,这与参与机构干预的序贯实施以及COVID-19大流行对患者就诊和管理的干扰有关。各机构的患者招募以及试验各阶段的时间存在相当大的异质性。试验末期干预组患者的招募也延长了,这可能引起一定程度的选择偏倚。为适应这种异质性(在数据揭盲后才充分认识到),我们事后决定根据日历时间而非试验阶段调整分析,这在另一项集群招募延迟的阶梯式楔形试验中也得到了推荐[31]。我们未发现随机组间患者特征或管理的实质性差异(总体及按地区),这对于去骨瓣减压术、机械通气和早期停止治疗的使用尤为重要,因为这些干预措施最有可能影响脑出血患者的生存率。即便如此,仍不能完全排除其他随时间变化的患者管理因素导致的未测量混淆。我们的试验未对次要结局的差异进行效能计算,次要结局的统计学显著性各不相同,且校正患者特征后通常无统计学意义。然而,所有次要结局的效应方向均一致支持治疗方案。在中低收入国家,干预实施、患者随访和数据质量监测存在后勤和实际问题。偏倚和测量误差可能影响基线和结局指标的评估,例如主要使用具有广泛社会人口学和文化背景的代理人评估患者的健康相关生活质量[43]。
总之,我们的试验结果为采用积极治疗方案提供了证据,即在急性脑出血症状出现后数小时内强化降压并联合管理关键异常生理指标,以改善患者的恢复。
参考文献出处见原文。原文链接如下:https://pmc.ncbi.nlm.nih.gov/articles/PMC10401723/
