
急性呼吸窘迫综合征(ARDS)是一种危及生命的炎症反应性疾病,以顽固性低氧血症和肺水肿为特征。尽管治疗手段不断进步,但ARDS仍具有高死亡率,其死亡原因多与全身炎症反应引发的多器官功能障碍综合征(MODS)相关。这是由原发事件相关的初始炎症级联反应与持续机械通气所致损伤之间复杂相互作用的结果,最终可导致多器官功能衰竭(MOF)乃至死亡。尽管近期研究日益强调胃肠道在此过程中的作用,但ARDS患者肠道功能障碍的病理生理机制仍未得到充分探索。本综述旨在阐明LI/ARDS患者肺与肠道之间的复杂相互机制,将系统探讨全身性炎症、上皮屏障功能障碍、机械通气(MV)的影响、高碳酸血症以及肠道菌群失调等多种因素。
肠道在危重症(包括创伤、胰腺炎、失血性休克、烧伤及ARDS)中具有重要影响,其通过调节全身炎症反应和脓毒症发病机制,在危重患者多器官功能障碍综合征(MODS)的病理生理过程中发挥关键作用。早期理论认为,危重症中肠道高通透性会导致细菌移位进入体循环。但现今学界普遍认识到,相关病理生理机制比既往认知更为复杂。事实上,危重症会全面影响肠道功能——包括上皮屏障、免疫系统及微生物组,从而可能启动病理性宿主反应。在机械通气患者中,可观察到肺部微生物组富含肠道相关菌群,这种现象与ARDS的发生存在关联。然而,LI/ARDS对患者肠道稳态及功能的影响尚未得到充分关注。
01ARDS患者全身炎症反应对肠道完整性的影响1ARDS患者全身炎症反应对肠道完整性的影响
ARDS患者体内持续升高的循环炎症因子和趋化因子标志着全身炎症反应的失调,这一过程被认为是导致多器官功能障碍的核心病理生理环节(图1)。事实上,ARDS的特征在于肺部与其他器官系统的双向交互作用,而非仅局限于呼吸系统,其本质是一种伴随炎症因子水平升高的全身性炎症状态。关键炎症介质的动态变化:在ARDS患者的支气管肺泡灌洗液(BALF)和血浆中均可检测到白细胞介素(IL)-1β、肿瘤坏死因子(TNF)-α、IL-6和IL-8等炎症因子的显著升高。这种异常的炎症反应不仅是患者短期及长期病死率的主要驱动因素,还会引发重要脏器的组织学改变,最终导致MODS的发生(图1)。
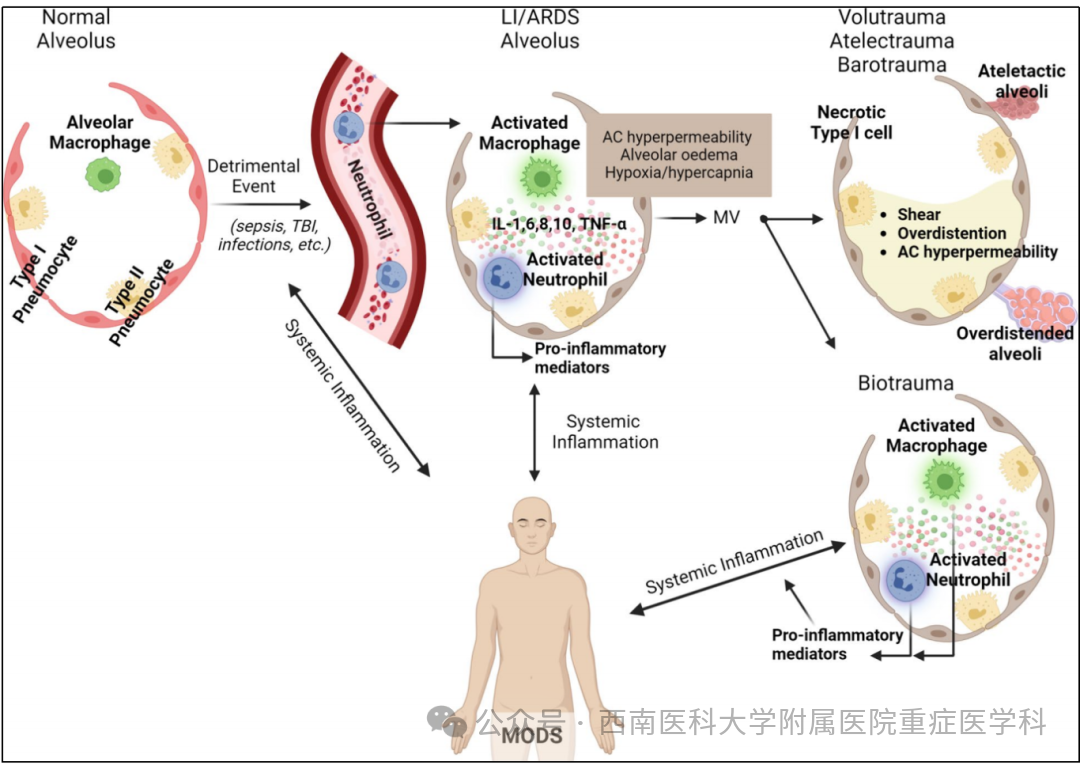
图1在患有LI/ARDS的患者中,肺毛细血管内皮受损,导致活化的免疫细胞迁移到肺部,从而加剧肺部炎症反应。在气腔内,肺泡巨噬细胞局部分泌细胞因子以诱导趋化作用并激活中性粒细胞,后者进而释放各种促炎分子。使用机械通气可能进一步加重肺损伤,可能导致过度的肺泡扩张(容积伤)、肺泡反复周期性的开闭(萎陷伤)以及复杂的炎症级联反应,导致局部和全身炎症(生物伤)。这种炎症可以扩展到远端器官和系统,加剧多器官功能障碍。ARDS急性呼吸窘迫综合征、IL白细胞介素、LI肺损伤、MODS多器官功能障碍综合征、MV机械通气、TBI创伤性脑损伤、TNF肿瘤坏死因子。
炎症细胞因子过度激活导致肠道屏障功能障碍:肠道通透性显著增加与脓毒症发生发展直接相关,并导致黏膜层完整性受损,表现为黏附力减弱、厚度减少和腔内覆盖减少。细胞因子风暴通过改变紧密连接的功能,特别是上调交联粘附分子(JAM)和紧密连接蛋白2,下调紧密连接蛋白5,以及紧密连接蛋白1、3、4、5和8的分布,导致肠道屏障功能障碍,破坏溶质的旁细胞转运并增加大分子的通透性(图2) 。此外,旁细胞高通透性还通过细胞因子激活肌球蛋白轻链激酶(MLCK)进一步介导,细胞因子通过前馈机制进一步放大MLCK活性,部分是通过改变紧密连接蛋白15(图2)。同样,在前瞻性队列研究中,脑外伤患者表现出严重的高细胞因子血症(IL-1β、IL-6、IL-8、IL-10和TNF-α)。脑外伤患者的TNF-α、IL-1β和IL-6水平升高会影响肠道紧密连接(TJ)的通透性。事实上,TNF-α与肠上皮细胞上的TNF受体(TNFRs)结合,启动与促炎细胞因子如核因子kB(NF-kB)相关的分子途径上调。此外,急性脑损伤后交感神经过度激活导致内脏灌注不足,进而引起肠TJ蛋白如闭合蛋白和闭合带蛋白-1(ZO-1)的变化,最终导致肠道高通透性(图2) 。
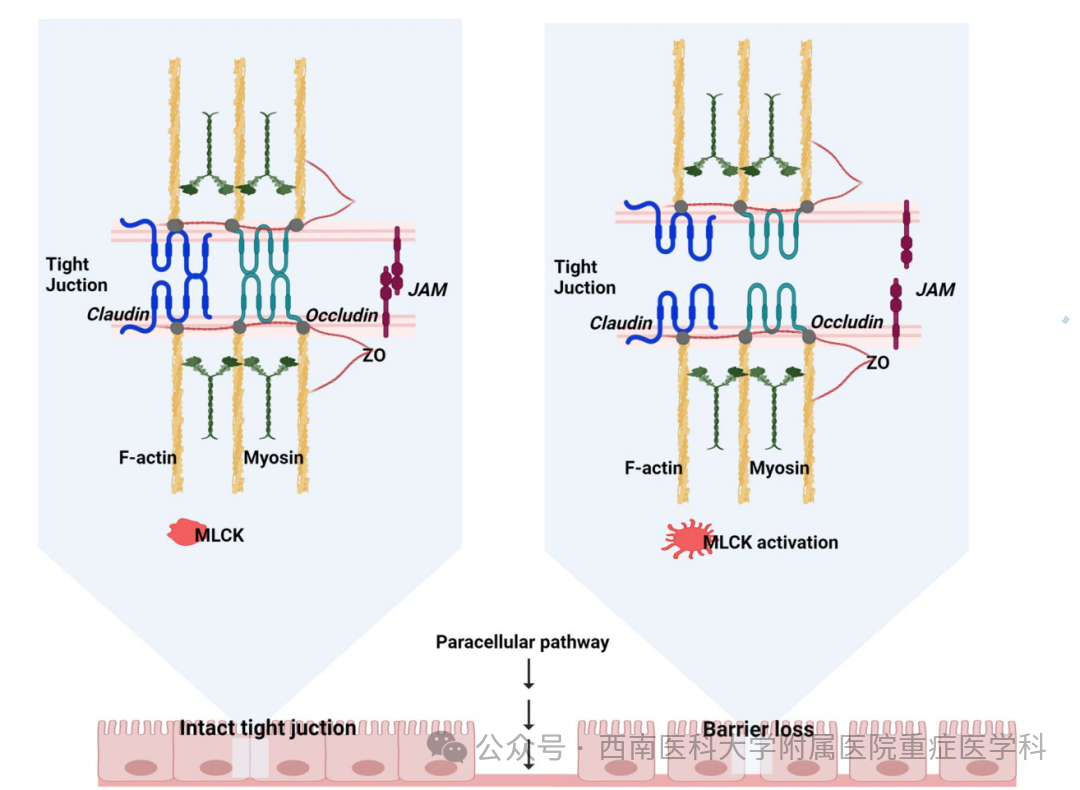
图2肠道在健康和重症中的作用。在重症情况下,紧密连接的完整性改变,这对于维持稳态至关重要,导致肠道完整性的丧失和通透性的增加。JAM结合黏附分子、MLCK肌球蛋白轻链激酶、ZO闭合蛋白
肠道菌群移位:肠道通透性受损可导致拟杆菌门和肠杆菌科等肠道微生物移位至ARDS患者肺部。这种细菌移位会激活黏膜免疫系统(MIS),促使炎症性化合物(危险相关分子模式-DAMPs)的产生,这些物质通过肠系膜淋巴管进入肺循环和体循环。当先天免疫细胞识别这些分子后,会进一步激活促炎通路,从而加速器官损伤(包括肠道损伤)和多器官功能障碍综合征(MODS)的进展。
02机械通气对肠道完整性的影响
尽管机械通气(MV)被视为ARDS治疗的基石之一,但认识到其可能加重肺损伤(LI)是ARDS研究领域的重大进展。这种被称为呼吸机相关性肺损伤(VILI)的现象涉及多种机制:(1)机械性损伤机制:跨肺压升高导致的压力伤,肺泡过度扩张引发的容积伤,肺泡周期性开闭造成的萎陷伤;(2)生物性损伤机制:机械力触发复杂炎症级联反应(生物伤),导致局部及全身炎症反应扩散;(3)系统性影响:炎症反应可波及远隔器官,系统加剧多系统器官功能障碍,最终导致病死率升高(图1、3)。
直到1998年,生物伤在呼吸机相关性肺损伤(VILI)发病机制中的作用才被阐明。在特定条件下,机械通气(MV)在维持气体交换的同时,可能引发炎症反应并导致继发性肺损伤。这些炎症级联反应可通过体循环扩散,影响肺外器官系统,最终导致多器官功能衰竭(MOF)。核心机制:(1)肺泡-血管通透性增加:MV促使炎症反应"去区域化",推动损伤从肺部向远端器官扩散(图1、3)。(2)双路径炎症触发机制:1)直接损伤路径:机械力导致细胞壁破坏,促炎细胞因子从肺泡局部释放入血;2)机械转导路径:已发现一种称为“机械转导”的机制,指的是细胞通过“机械感觉”过程检测机械力,并将其转化为一系列细胞信号事件,即“机械转导”。体外研究表明,大多数肺细胞在受到周期性拉伸时可以产生细胞因子。(3)DAMPs介导的恶性循环:机械损伤会导致DAMPs的释放,进而触发免疫细胞的募集,这些细胞会产生促炎细胞因子。同时,由于过度拉伸导致肺泡上皮细胞和血管内皮细胞信号级联的激活,以及神经炎症反射的失调,会引发强烈的全身性炎症反应。(4)临床影响:大潮气量(TV)MV持续施加有害机械力,形成"炎症-通透性增加-易损性升高"的恶性循环。
现有证据表明,呼吸机介导的炎症反应可波及肝脏、肾脏及大脑等远端器官,但VILI对肠道完整性的损伤效应仍知之甚少。目前存在以下研究:(1)炎症因子对肠道屏障的影响:TNF-α、IL-1β和IL-6可显著改变肠道紧密连接(TJ)通透性,Guery等(2003)证实:MV升高血浆TNF水平及肠道通透性,TNF中和抗体可逆转肠道高通透性。(2)TNF-α的损伤机制:TNF-α引起的肠上皮屏障功能障碍的潜在机制复杂多样:诱导肠上皮细胞凋亡、改变细胞膜脂质组成、钙-钙调蛋白激活MLCK、通过增加MLCK蛋白表达刺激肌球蛋白轻链(MLC)磷酸化以及抑制紧密连接蛋白表达。值得注意的是,MLCK介导的MLC磷酸化途径在TNF-α引起的肠上皮屏障功能障碍发展中起着关键作用。(3)IL-6的双重作用争议:虽在全身/局部炎症中起关键作用,关于IL-6是对肠屏障产生保护作用还是破坏作用存在争议。(4)最新动物模型证据:Ding等(2020)通过VILI小鼠模型发现血清和肠道组织中TNF-α、IL-1β、IL-6水平升高(ELISA检测),出现"PANoptosis"现象(凋亡+焦亡+坏死性凋亡共存),伴随occludin/ZO-1表达下降,claudin-2表达升高,MLC激活;气管内给予Imp7siRNA纳米颗粒可抑制细胞因子产生,减轻VILI肠道损伤。(5)呼吸策略的影响:Imai等(2003)酸吸入ARDS兔模型显示高潮气量+零PEEP通气策略显著增加肾/小肠上皮细胞凋亡,与器官功能障碍程度正相关。
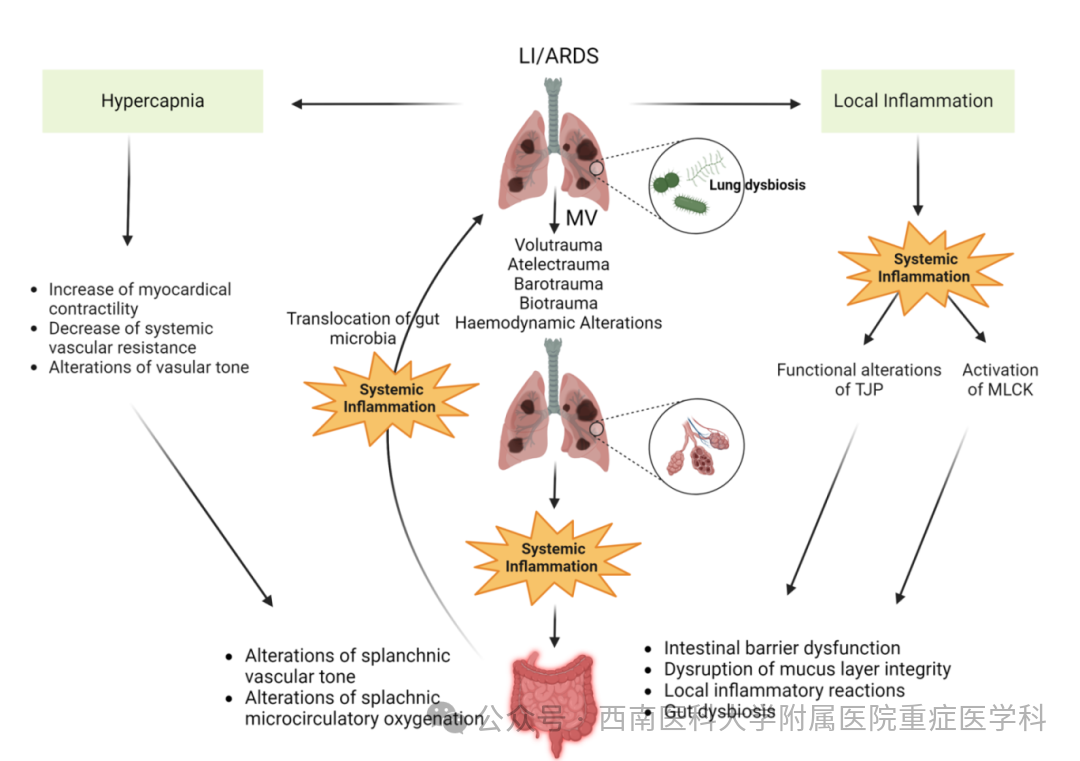
图3在患有LI/ARDS的患者中,严重的急性炎症导致紧密连接蛋白的功能改变和MLCK激活,这些变化与肠屏障功能障碍、黏液层完整性破坏、肠道炎症反应加剧以及肠道菌群失调有关。机械通气可能引起VILI,进一步加重全身炎症和肠道损伤。低潮气量机械通气和保护性机械通气引起的高碳酸血症期间的血流动力学改变与心肌收缩力增加、全身血管阻力降低及血管张力改变有关,导致内脏血管张力和内脏微循环氧合的变化。肠道功能障碍和肠壁完整性丧失会增强全身炎症,并促进肠道细菌移位至肺部,恶化已有的由LI介导的肺部菌群失调。ARDS急性呼吸窘迫综合征、LI肺损伤、MLCK肌球蛋白轻链激酶、MV机械通气、TJP紧密连接蛋白、VILI机械通气诱导的肺损伤。
03从机械角度考虑机械通气的影响
(1)肺保护性通气的核心地位
循证支持:低潮气量(TV)+高PEEP策略可降低ARDS病死率,成为标准治疗方案。
现存矛盾:PEEP对内脏灌注及血流动力学的影响存在争议性数据。
(2)PEEP的负面血流动力学效应
机制:静脉回流减少 → 心输出量降低(与PEEP水平正相关),无肺损伤患者机械通气时,PEEP≥10cmH₂O即可显著降低心输出量。
手术患者数据:PEEP从0升至15cmH₂O时混合静脉及肝静脉血氧饱和度同步下降, 门静脉血流减少,但内脏氧摄取代偿性增加。
(3)脓毒症相关肺损伤的特殊性
PEEP=15cmH₂O时:心输出量下降+ 肝静脉氧饱和度下降(较10cmH₂O差异显著)。
剂量依赖性效应:
PEEP<10 cmH₂O:内脏血流影响轻微
PEEP=15-20 cmH₂O:内脏灌注显著降低机械通气(MV)影响肠道功能存在多种机制,尽管前文重点探讨了MV通过内脏灌注减少和全身血流动力学改变影响肠道完整性,但其对肠道功能的影响实则涉及多因素交互作用:1)肾素-血管紧张素-醛固酮系统(RAAS)激活:MV升高血浆RAAS活性,加剧内脏缺血。2)交感神经过度兴奋:儿茶酚胺释放增加,进一步减少内脏血流。3)MV常用辅助药物可能加重肠道功能障碍:阿片类药物抑制胃肠蠕动,镇静剂(如苯二氮䓬类)过静脉扩张作用减少静脉回流,降低血管活性药物反应性。
04高碳酸血症在肺肠道轴中的作用
急性呼吸衰竭与高碳酸血症对多器官灌注的复杂影响:
(1) 呼吸衰竭的全身性挑战
急性呼吸衰竭不仅导致气体交换障碍,还通过以下机制增加心血管系统负担:
高心输出量需求:为代偿低氧血症而增加氧输送
右心室后负荷升高:缺氧性肺血管收缩→肺萎陷→肺动脉压力升高
氧耗增加:呼吸肌做功增加及气体交换效率下降
(2)肺保护性通气与高碳酸血症的双刃剑效应
低潮气量(TV)通气虽可减轻肺损伤(LI/ARDS),但常导致允许性高碳酸血症,其心血管影响呈现多向性(图3)
正向作用:
交感神经激活→心肌收缩力增强
全身血管阻力降低→心输出量增加
器官特异性血流重分布:
肺/肾脏:局部血管收缩
脑:血管扩张
(3) 内脏血流的动态变化
高碳酸血症对肝/内脏血流呈双相调节:
早期阶段:交感兴奋主导→内脏血流减少
后期阶段:CO₂直接扩血管效应→血流代偿性增加
临床观察:
稳定机械通气患者中,动脉PCO₂适度升高可改善全身灌注
但胃粘膜-动脉PCO₂差值(DPCO₂)未见显著变化
在ARDS患者中,尽管肺保护通气策略导致心输出量增加,但未能改善胃黏膜灌注。据推测,低TVMV导致的个体胃黏膜灌注变化的变异性表明,组织PCO2升高引起的局部血管扩张可能被系统循环中儿茶酚胺释放增加所抵消。
05缺血/再灌注损伤对肠道完整性的影响
Deitch于2002年提出"三次打击"模型,系统阐述危重症中肠道损伤的级联反应:(1)首次打击(初始损伤):内脏低灌注(如休克、创伤),导致肠道释放促炎介质,启动炎症反应;(2)二次打击(再灌注损伤):血流动力学复苏,其病理变化包括缺血-再灌注损伤,非依赖于细菌/毒素易位的肠道屏障功能丧失,肠源性炎症反应放大;(4)三次打击(全身炎症爆发):细菌/内毒素突破黏膜屏障,诱导释放趋化因子、细胞因子等炎症介质(图3),局部及全身免疫系统激活,最终导致全身炎症反应综合征(SIRS),多器官功能障碍综合征(MODS)。最后,如前所述,在危重疾病中,黏液层受损,导致上皮细胞功能障碍。缺血/再灌注事件进一步加剧了这一问题,降低了黏液层的疏水性,并导致肠通透性变化。06肺微生物组改变对肠道完整性的影响
肺-肠微生物组交互:从基础到临床的认知演进
(1)肺部微生物组认知的范式转变
传统观念突破:曾认为肺部是无菌环境,阻碍了相关研究进展
现有证据表明:健康人群普遍存在微误吸/胃食管反流现象,气管隆突是细菌DNA最密集区域(密度随支气管分级递减)。
健康下呼吸道菌群特征:
以普雷沃菌、韦荣球菌、链球菌和梭杆菌为主。
(2) 危重症对微生物组的重塑
ICU干预措施的影响:机械通气、抗生素、血液净化等改变微生物组成。
ARDS患者的特征性改变:1)细菌多样性降低(α多样性指数下降);2)肠道来源菌(如肠杆菌科)在肺部定植增加;3)与IL-6/IL-8等炎症介质升高显著相关
(3) 肺-肠轴的交互作用
肺病影响肠道菌群:1)流感病毒感染导致肠道肠杆菌科增加,乳酸菌减少;2)COVID-19患者肠道菌群紊乱:机会致病菌增加/有益共生菌降低。
肠道菌群影响肺损伤:1)休克动物模型中,肠道抗生素预处理可预防肺损伤;2)肺源性CCR9+CD4+T细胞通过IFN-γ改变肠道菌群;3)I型干扰素依赖的菌群调控机制。
(4)关键病理机制
肺泡-毛细血管通透性增高:促进细菌跨器官易位(图1,3)
黏液屏障破坏:1)疏水性下降→水溶性毒素穿透;2)缺氧环境促进变形菌门(含铜绿假单胞菌、大肠杆菌)增殖
"致病微生物组"的形成:紧密连接破坏+黏液完整性丧失→胃肠损伤→MODS
尽管越来越多的证据表明肺微生物组的变化可能会影响肠道完整性,但我们对ARDS中肺菌群失调如何特异性影响肠道微生物群的理解仍存在显著差距。进一步的研究对于阐明这些途径及其临床相关性至关重要。
07 治 疗
1.肠-肺轴与微生态干预:ARDS治疗新视角
(1)肠道微生态的核心地位
鉴于肠-肺轴与肠道屏障完整性对危重症的深远影响,针对微生物组的干预策略有望改善ARDS患者预后。其中,肠道细菌代谢产物(尤其是短链脂肪酸SCFAs)通过调控局部和全身免疫应答,成为益生菌/益生元发挥免疫调节作用的关键介质。
(2)益生元的双重作用机制
定义:以不可消化寡糖为主的膳食成分,选择性促进有益菌(如双歧杆菌)生长
功能特性:1)发酵产物:肠道微生物发酵单糖聚合物产生SCFAs、肽聚糖等,调节先天免疫;2)临床价值:减轻肠道炎症、内毒素血症及高细胞因子血症; 维持黏膜免疫稳态与屏障完整性。
(3)益生菌的多靶点效应
定义:足量摄入时对宿主有益的活菌(含乳酸菌、酵母菌等)。
作用谱系:
功能类别 | 具体机制 |
物理屏障维护 | 增强紧密连接,减少细菌易位 |
微生物平衡 | 竞争性抑制致病菌(如金黄色葡萄球菌)定植 |
免疫调控 | 降低促炎因子(TNF-α/IL-6),提升抗炎因子(IL-10) |
代谢改善 | 降低尿素毒素,优化脂质代谢 |
2.粪菌移植(FMT)与精准微生态调控:ARDS治疗新方向
(1)FMT在危重症中的治疗潜力
通过将健康供体的粪便菌群移植至肠道菌群失调患者,FMT已证实可通过以下机制改善危重症预后:1)恢复肠道菌群多样性;2)抑制致病菌过度增殖(如肠杆菌科);3)促进共生菌的竞争性定植;4)重建宿主免疫稳态。
(2)未来研究的范式转变
需从传统对症治疗(如肺保护性通气)转向更精准的干预策略:
核心目标:恢复肠-肺轴生态平衡;同步保护肺/肠道微生物组稳定性
关键途径:调控肠道菌群组成,增强肠道屏障完整性
预期效益:减少细菌/内毒素易位,降低ARDS发病率及严重程度,改善相关肠功能障碍
(3)多机制协同作用
干预层面 | 具体效应 |
微生物组重塑 | 增加SCFAs产生菌(如普雷沃菌),抑制病原体定植 |
屏障修复 | 上调occludin/ZO-1表达,降低肠道通透性 |
免疫调节 | 平衡促炎/抗炎因子(如降低IL-6,升高IL-10) |
代谢调控 | 减少尿素毒素积累,改善肠-肝轴功能 |
08 结 论
肠-肺轴被认为是ARDS病理生理学中的关键组成部分,强调了细菌和免疫在肠道与肺部之间双向交流的重要性。每个领域和区域都在这一相互作用中发挥着核心作用,从而影响LI/ARDS的预后。在保护性通气和维持全身血流动力学之间,旨在恢复肠道完整性、微生物群以及两个系统之间稳态平衡的潜在疗法,可能对LI/ARDS的管理产生重要贡献。虽然肠-肺轴在ARDS病理生理中被认为至关重要,但仍需进一步研究以阐明肠道与肺部相互作用的双向途径及其在肺部和肺外损伤中的作用。这种理解对于开发旨在维持肠壁完整性、微生物群和稳态的疗法,有效管理LI/ARDS至关重要。
